1、选择题 下列说法正确的是( )
A.一种烃在足量的氧气中完全燃烧后的产物通过碱石灰,减少的体积就是生成的二氧化碳的体积(温度>100℃)
B.某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的C:H=1:2
C.某气态烃CxHy与足量O2完全反应,如果反应前后气体体积不变(温度<100℃),则y=4;若体积减少,则y<4;否则y>4
D.相同质量的烃,完全燃烧,消耗O2越多,烃C:H越大
参考答案:B
本题解析:
本题难度:一般
2、简答题 TMB是一种应用指纹检测新型安全的色原试剂.已知TMB中含有碳、氢、氮三种元素,其相对分子质量为240.为测定TMB的组成,用下列各仪器装置,在过量的氧气流中4.80gTMB样品氧化成CO2、H2O和N2,再利用吸收剂分别吸收水和二氧化碳,以确定其中所含碳、氢、氮原子的比例关系.请从下图中选择适当的装置(装置符合气密要求,加热装置等已略去;其他用品可自选).

(1)将所选用的仪器(可重复选用)连接顺序由上到下依次填入下表,并写出该仪器中应加的试剂的名称及作用.
| 选用的仪器 | 加入试剂 | 加入试剂的作用
C
H2O2溶液与MnO2
产生氧气
D
CuO
保证C全部转化为CO2
|
(2)实验后称得A装置从用的先后顺序排列质量分别增加3.60g、14.08g、0.14g,则TMB的分子式为______.
参考答案:(1)实验原理:将TMB用氧气氧化为二氧化碳、水和氮气,再利用吸收剂分别吸收水和二氧化碳,以确定其中所含碳、氢、氮原子的比例关系.在整个实验中,要求碳元素全部以二氧化碳形式出现,因此在氧化后需要用氧化铜作最后保障;为防止氧气产生时所带水蒸气的影响,要先对氧气进行干燥,选择干燥剂需考虑所提要求“实验后称得A装置从用的先后顺序排列质量分别增加3.60g和14.08g”,因此干燥氧气选择干燥剂B;利用吸收剂分别吸收水和CO2需考虑试剂影响,先吸收水后吸收CO2,则连接顺序为:
选用的仪器加入试剂加入试剂的作用CH2O2溶液与MnO2产生氧气B浓H2SO4干燥氧气DTMBTMB氧化成CO2、H2O和N2DCuO保证C全部转化为CO2ACaCl2吸收水分ANaOH吸收CO2A碱石灰防止空气中的CO2和H2O进入装置中故答案为:
选用的仪器加入试剂加入试剂的作用CH2O2溶液与MnO2产生氧气B浓H2SO4干燥氧气DTMBTMB氧化成CO2、H2O和N2DCuO保证C全部转化为CO2ACaCl2吸收水分ANaOH吸收CO2A碱石灰防止空气中的CO2和H2O进入装置中(2)实验后称得A装置从用的先后顺序排列质量分别增加3.60g、14.08g、0.14g,则m(H2O)=3.60g,m(CO2)=14.08g,而0.14g为空气中的CO2和H2O进入装置中的质量,则
n(H2O)=3.60g18g/mol=0.2mol,n(H)=0.4mol,m(H)=0.4g,
n(CO2)=14.08g44g/mol=0.32mol,n(C)=0.32mol,m(C)=0.32mol×12g/mol=3.84g,
所以m(N)=4.80g-0.4g-3.84g=0.56g,
n(N)=0.56g14g/mol=0.04mol,
则:n(C):n(H):n(N)=0.32mol:0.4mol:0.04mol=16:20:2,
所以分子式为C16H20N2,
故答案为:C16H20N2.
本题解析:
本题难度:一般
3、简答题 为测定某含有杂质Na2O的Na2O2样品的纯度,3个小组分别设计如下方案.首先准确称量样品mg,然后,按照以下方案进行实验:
[方案一]:将样品与水充分反应,使产生的O2通过灼热的铜粉,测得反应后生成氧化铜的质量为ng,通过计算求出试样中Na2O2的含量.此方案测定的结果误差较大,主要原因是:______;
[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量.
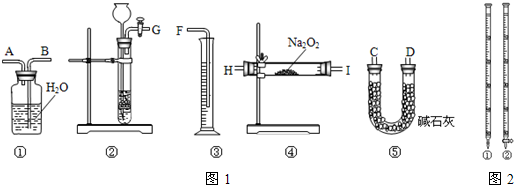
(1)按此方案,以下制取CO2和实验使用的仪器的连接次序是______.(填写如图1所示仪器编号)
(2)装置⑤的作用是:______.
[方案三]:测定样品与水充分反应后溶液的体积Vml,再从中取V1mL溶液,装入锥形瓶,用标准浓度的盐酸进行滴定,确定溶液的浓度,再计算出样品中Na2O2的含量.
(1)此方案中酸碱滴定时,选用的滴定管为______(填如图2所示仪器编号).
(2)若用甲基橙做指示剂,达到滴定终点时的现象为______.你认为方案二、方案三中测定结果比较准确的是______.
参考答案:方案一:将样品与水充分反应,使产生的O2通过灼热的铜粉,测得反应后生成氧化铜的质量为ng,通过计算求出试样中Na2O2的含量,过程中铜粉不一定全部都变成了
氧化铜,所以会产生误差,
故答案为:O2与Cu反应时难于全部转化成CuO;
方案二:
(1)将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量,实验装置设计为先利用装置②制备二氧化碳,通过装置④和样品中过氧化钠反应,通过装置⑤除去过量的二氧化碳,利用①③采取排水量气方法测定生成氧气的体积,导管应短进长出;仪器的连接顺序为:②④⑤①③,
故答案为:仪器的连接次序是③④⑤①③;
(2)装置⑤是利用碱石灰除去氧气中过量的二氧化碳气体,避免影响氧气的体积测定,
故答案为:除去O2中混有的CO2气体;
方案三:
(1)此滴定实验是利用盐酸滴定氢氧化钠溶液,标准溶液盐酸盛在酸式滴定管中进行滴定实验,故答案为:②;
(2)甲基橙做滴定指示剂,滴定终点是溶液有黄色变化为橙色且半分钟不变化;方案一中铜不一定全部变化为氧化铜,方案二中,装置中的气体不一定全部赶出,方案三是精确测定待测溶液的浓度结果较准确,
故答案为:溶液颜色由黄变橙且半分钟不变色;最准确的是方案三.
本题解析:
本题难度:一般
4、选择题 下列实验操作示意图所示的实验操作正确的是
?[? ]
A.加热结晶水合物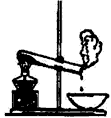
B.镁条在二氧化碳中燃烧 
C.制备较纯净的HF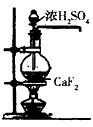
D.红磷转变成白磷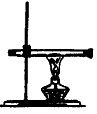
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列物质不能用于从碘水中提取碘的是
[? ]
A.乙醇
B.苯
C.四氯化碳
D.直馏汽油
参考答案:A
本题解析:
本题难度:简单