|
高考化学知识点整理《化学反应与能量》试题特训(2017年最新版)(八)
2017-11-05 22:32:12
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、选择题 下列对化学反应的认识错误的是
A.会引起化学键的变化
B.会产生新的物质
C.必然引起物质状态的变化
D.必然伴随着能量的变化
|
参考答案:C
本题解析:化学反应的本质是旧化学键的断裂和新化学键的形成,且生成新物质,A、B正确;化学反应不一定能引起物质状态的变化,C错误;任何一个化学变化必定伴随着能量的变化,常以热量的形式表现出来,D正确,答案选C.
考点:化学变化的实质
本题难度:一般
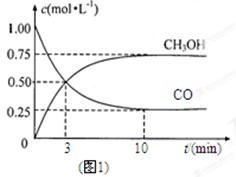
2、填空题 工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) 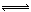 CH3OH(g)。 CH3OH(g)。
(1)图1是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)= ; H2的平衡转化率为_________________________。
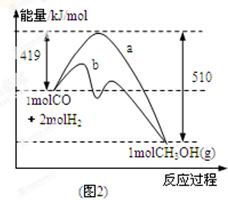
(2)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。写出反应的热化学方程式 。
(3)该温度下,反应平衡常数K=______________(填数值),温度升高,平衡常数K_________(填“增大”、“不变”或“减小”)。
(4)恒容条件下,下列措施中能使反应体系中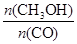 增大的措施有 。 增大的措施有 。
a.升高温度 b.充入He气 c.再充入2 molH2 d.使用催化剂
参考答案:(11分)
(1)0.075mol・L-1・min-1(2分) 0.75(或75%)(2分)
(2)CO(g) + 2H2(g)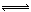 CH3OH(g) ΔH=-91 kJ・mol-1(2分) CH3OH(g) ΔH=-91 kJ・mol-1(2分)
(3)4 mol-2・L-2(2分) 减小 (1分)
(4)C(2分)
本题解析:(1)由图可知,CO浓度变化量为1.00mol/L-0.25mol/L=0.75mol/L,△t=10min,则v(CO)=0.75mol/L÷10min=0.075mol/(L?min),氢气的平衡转化率为1.5/2=0.75。
(2)反应物的总能量为419kJ,生成物的总能量为510kJ,则该反应为放热反应,放出的热量为419kJ-510kJ=91kJ,热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol,该反应使用催化剂,只能改变反应的途径降低反应所需的活化能,而不能改变反应热,故答案为:放热;CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol;不能;
(3) CO(g)+2H2(g)?CH3OH(g)
初始浓度(mol/L): 1 2 0
转化浓度(mol/L): 0.75 1.5 0.75
平衡浓度(mol/L): 0.25 0.5 0.75
平衡常数K="0.75/(0.75" ×0.52 )=4mol-2・L-2
因该反应为放热反应,则升高温度,化学平衡逆向移动,K值减小;
(4)使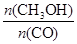 增大,化学平衡应正向移动,但升高温度时化学平衡逆向移动,恒容条件下充入He气化学平衡不移动,使用催化剂化学平衡不移动,在恒容条件下再充入1molCO和2molH2,压强增大,化学平衡正向移动,符合题意,故c正确,故答案为:c。 增大,化学平衡应正向移动,但升高温度时化学平衡逆向移动,恒容条件下充入He气化学平衡不移动,使用催化剂化学平衡不移动,在恒容条件下再充入1molCO和2molH2,压强增大,化学平衡正向移动,符合题意,故c正确,故答案为:c。
考点:本题考查的是化学原理知识,涉及化学反应速率计算、转化率计算、平衡常数的计算、热化学方程式的书写、平衡常数的应用等。
本题难度:困难
3、选择题 下列反应的离子方程式书写正确的是
A.氯气通入氢氧化钠溶液中:Cl2+2OH-=Cl-+ClO-+H2O
B.稀硫酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑
C.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓
D.氯化铁溶液与铜粉反应:Cu+Fe3+=Fe2++Cu2+
参考答案:A
本题解析:分析:A.反应生成氯化钠、次氯酸钠、水;
B.反应生成硫酸亚铁和氢气;
C.漏写生成水的离子反应;
D.电荷不守恒.
解答:A.氯气通入氢氧化钠溶液中的离子反应为Cl2+2OH-=Cl-+ClO-+H2O,故A正确;
B.稀硫酸与铁粉反应的离子反应为Fe+2H+=Fe2++H2↑,故B错误;
C.氢氧化钡溶液与稀硫酸反应的离子反应为SO42-+2H++2OH-+Ba2+=2H2O+BaSO4↓,故C错误;
D.氯化铁溶液与铜粉反应的离子反应为Cu+2Fe3+=2Fe2++Cu2+,故D错误;
故选A.
点评:本题考查离子反应的书写,注意离子方程式的书写规则和各离子的电荷是否守恒,明确沉淀、气体、水在离子反应中保留化学式即可解答,题目较简单.
本题难度:困难
4、选择题 化学反应速率最主要取决于 ? ? ? ? ? ? ? ? ? 。
A.是否使用催化剂
B.反应物的性质
C.反应的温度
D.反应的压强
参考答案:B
本题解析:试题分析:化学反应速率最主要取决于反应物的性质,即内因,B正确,强于选项都是外因,答案选B。
考点:考查影响反应速率因素的判断
点评:该题的关键是明确影响反应速率的因素分为内因和外因两种,但决定性因素是内因,有利于培养学生的逻辑推理能力和灵活应变能力。
本题难度:一般
5、填空题 Ⅰ.氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol 请回答下列问题:
(1)生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和
(2)若2 mol氢气完全燃烧生成水蒸气,则放出的热量 572 kJ(填“>”、“<”或“=”)
Ⅱ.已知1molCu(s)与适量O2(g)发生反应,生成CuO(s),放出157kJ热量。写出该反应的热化学方程式 。
参考答案:Ⅰ.(1)小于 (2)< Ⅱ.Cu(s)+1/2O2(g)=CuO(g) △H=-157kJ/mol
本题解析:Ⅰ.(1)氢气燃烧是放热反应,所以生成物的总能量小于反应物的总能量。
(2)应用气态水的能量高于液态水的能量,因此氢气燃烧生成液态水时放出的能量多,则2 mol氢气完全燃烧生成水蒸气,则放出的热量<572 kJ。
Ⅱ.已知1molCu(s)与适量O2(g)发生反应,生成CuO(s),放出157kJ热量,则该反应的热化学方程式Cu(s)+1/2O2(g)=CuO(g) △H=-157kJ/mol。
考点:考查反应热的计算以及热化学方程式的书写
点评:该题是基础性试题的考查,难度不大。明确反应热与反应物和生成物总能量的相对大小是答题的关键。有利于培养学生的逻辑推理能力和规范答题能力。
本题难度:一般
|