1、选择题 使用单质铜制硝酸铜,耗用原料最经济,而且对环境几乎没有污染的是(?)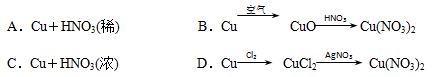
参考答案:B
本题解析:A、B、C、D发生的反应分别为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;2Cu+O2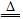 2CuO、CuO+2HNO3=Cu(NO3)2+H2O;Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;Cu+Cl2
2CuO、CuO+2HNO3=Cu(NO3)2+H2O;Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;Cu+Cl2 CuCl2、CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2。生成等物质的量的硝酸铜消耗硝酸最少的是方案B,而且B方案无污染。D方案需使用氯气,氯气是有毒气体而且硝酸银价格昂贵,不经济。
CuCl2、CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2。生成等物质的量的硝酸铜消耗硝酸最少的是方案B,而且B方案无污染。D方案需使用氯气,氯气是有毒气体而且硝酸银价格昂贵,不经济。
点评:评价化学实验方案的优劣一般考虑:有无污染、消耗原料多少、原料来源是否广泛、原料是否廉价等。
本题难度:一般
2、选择题 将盛有N2和NO2的混合气体的试管倒立于水中经过充分反应后,气体体积减少为原来的一半,则原混合气体中N2和NO2的体积比是
A? 1:1? B? 1:2?C? 1:3? D ?3:1
参考答案:C
本题解析:设N2和NO2的体积分别为a、3b,3b体积的NO2与水反应生成b体积的NO,则a+3b=2(a+b),a=b,C正确。
本题难度:一般
3、选择题 下列叙述中正确的是
A.实验室制取氨气的发生装置与用高锰酸钾制取氧气的装置相同
B.并不是所有的铵盐都能与烧碱共热生成氨气
C.除去NO中混有的少量NO2,可将混合气体通过盛有水的洗气瓶,再用排空气法收集NO
D.CO2、NO2、P2O5均与水反应生成酸为酸性氧化物
参考答案:A
本题解析:实验室制取氨气用NH4Cl与Ca(OH)2混合加热反应,所以均是固固需要加热的反应,制取装置相同,A选项正确;C选项再用排空气法收集NO,NO与空气中的氧气反应,错误;NO2不属于酸性氧化物,D选项错误。
本题难度:一般
4、选择题 工业以CaO和硝酸反应制Ca(NO3)2・4H2O晶体,为确保制备过程既不补充水分,又无水剩余,则应选用的硝酸质量分数为?
A.30%
B.70%
C.63%
D.84%
参考答案:B
本题解析:根据方程式CaO+2HNO3=Ca(NO3)2+H2O可知,如果生成1molCa(NO3)2・4H2O,则需要氧化钙和硝酸分别是1mol和2mol,反应中还同时还生成1mol水。这说明原溶液中含有的水是3mol,则硝酸的质量分数是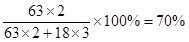 ,答案选B。
,答案选B。
本题难度:简单
5、选择题 为除去镀在铝制品表面的铜镀层,可选用的试剂是(?)
A.稀硝酸
B.浓硝酸
C.浓硫酸
D.浓盐酸
参考答案:B
本题解析:稀硝酸既能溶解铜,也能溶解铝,不符合要求。浓硝酸在常温下可溶解铜,不能溶解铝(钝化),符合要求。浓硫酸在常温下既不能溶解铜,也不能溶解铝;在加热条件下既能溶解铜,也能溶解铝,不符合要求。浓盐酸不能溶解铜,能溶解铝,不符合要求。
本题难度:简单