1、选择题 在由Fe、FeO和Fe2O3组成的混合物中加入100?mL?2?mol・L-1的盐酸,恰好使混合物完全溶解,并放出448?mL气体(标准状况),此时向溶液中滴加KSCN溶液无现象。则下列判断正确的是
[? ]
A.混合物中三种物质反应时消耗盐酸的物质的量之比为1∶1∶3
B.反应后所得溶液中的Fe2+和Cl-的物质的量之比为1∶3
C.混合物中,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多0.02?mol
D.混合物中,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多0?.01?mol
2、计算题 某学生用NaHCO3和KHCO3组成的某混合物进行实验,现称取不同质量的混合物溶于水后,分别滴入相同浓度的盐酸50 mL,产生CO2气体的体积(标准状况)如下图 所示
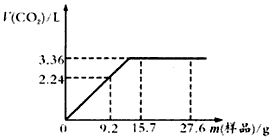
(1)求所用盐酸的物质的量浓度;
(2)求混合物中NaHCO3的质量分数。
3、选择题 由Zn、Fe、Al、Mg四种金属中的两种组成的混合物13g,与足量的盐酸反应产生的氢气在标况下为11.2升,则混合物可能的组成是
[? ]
A.Zn和Fe
B.Fe和Al
C.Al和Mg
D.Mg和Fe
4、选择题 将标准状况下体积为224.0mL的Cl2通入到25.0mL?0.1mol/LNa2S2O3溶液中恰好完全反应,此时Cl2全部转化为Cl-,则S2O32-转化为
[? ]
A.SO42-?
B.SO32-?
C.S?
D.S2-
5、计算题 有硫酸钾和碳酸镁的混合物,用50?mL?盐酸完全溶解后,在标准状况下收集到0.56L二氧化碳,向反应后的溶液中加入含有0.03?mol氢氧化钡的溶液,可得到6.11g沉淀,此时溶液中的c(OH-)=0.01mol/L,溶液的体积为200mL,试求:(要求有必要的解题过程)
(1)?原混合物中碳酸镁的质量 ?
(2)?得到的沉淀中硫酸钡的质量 ?
(3)?盐酸的物质的量浓度