1、选择题 第三周期元素的原子,其最外层p能级上仅有一个未成对电子,它最高价氧化物对应的水化物的酸根离子是
A.RO
B.RO
C.RO
D.RO
参考答案:D
本题解析:略
本题难度:一般
2、选择题 金属元素原子的最外层电子数为m,非金属元素原子的最外层电子数为n,则m与n的关系是(?)
A.大于
B.小于
C.等于
D.不能肯定
参考答案:D
本题解析:金属元素的原子最外层电子数少于4个,非金属元素的原子最外层电子数多于4个,这仅仅是一般规律。有个别非金属元素如氢元素原子最外层电子数为1,个别金属元素如铋最外层电子数为5,故m与n的关系不能确定。
本题难度:简单
3、选择题 如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是?
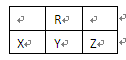
A.X的氢化物比R的氢化物稳定
B.原子半径大小顺序是Z>Y>X
C.Y、R形成的化合物YR2能使KMnO4溶液褪色
D.X、Z可形成化合物XZ5,分子中各原子均满足最外层8电子结构
参考答案:C
本题解析:X为2、8、5结构,是P,从而推出Y为S,Z为Cl,R为O,然后根据元素周期律来进行推导。
本题难度:一般
4、选择题 四种短周期元素W、X、Y、Z的原子序数依次递增,X的一种单质能在空气中自燃。电解含有Y和Z的阴离子的混合溶液时,在阳极Y离子先失去电子。W和Z同主族。对于这四种元素下列判断正确的是
A.气态氢化物的稳定性:W>X>Y>Z
B.单质的氧化性:W>Z>Y>X
C.四种元素原子半径大小:W<Y<Z<X
D.W单质可以将Z从其盐溶液中置换出来
参考答案:B
本题解析:由X的一种单质易自燃可知,X为磷元素,则Y、Z分别为S、Cl,进而由Cl可知W为氟元素。元素非金属性越强其气态氢化物的稳定性越强,因此四种元素的气态氢化物稳定性:F>Cl>S>P,A错;单质的氧化性:F2>Cl2>S>P,B正确;同周期元素原子半径随核电荷数增大而减小,故原子半径:P>S>Cl>F,C错;F2因可与H2O反应,故F2不能从氯化物中置换出氯气,D错
本题难度:简单
5、填空题 Ⅰ.通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示四种微粒:A________,B________,C________,D________。
(2)写出A、B、E三种微粒反应的离子方程式:____________________________________________________。
Ⅱ.(1)CH3+、CH3-、CH3-都是重要的有机反应中间体,它们的电子式分别是________、________、________;其中CH3+中四个原子是共平面的,三个键角相等,则键角应是________。
(2)叠氮化合物在化学工业上有重要应用。N3-叫做叠氮离子,请写出由三个原子构成的含有与N3-的电子数相同的粒子的化学式(3种)________、______、_______。
参考答案:Ⅰ.(1)H2O NH3 NH4+ OH-
(2)Al3++3NH3+3H2O=Al(OH)3↓+3NH4+或Mg2++2NH3+2H2O=Mg(OH)2↓+2NH4+
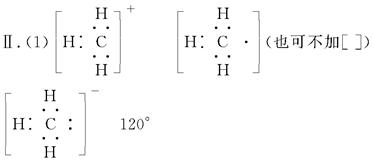
(2)CO2 N2O BeF2
本题解析:Ⅰ.以Ne为基本出发点,依题意找出等电子微粒解答。
Ⅱ.(1)由电子式书写规则写出电子式,(2)利用等电子原理找出符合题意的物质。
本题难度:一般