1、选择题 下列叙述中,正确的是
A.CH4的摩尔质量为16
B.等质量的O2和O3中所含的氧原子数不相同
C.0.2?mol?L-1Na3PO4溶液中Na+的物质的量浓度是0.6?mol?L-1
D.24?g?Mg与足量稀盐酸反应转移的电子数约为6.02×1023
参考答案:C
本题解析:分析:A.摩尔质量的单位是g/mol;
B.氧气和臭氧属于同分异构体,组成元素相同,根据N=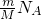 计算;
计算;
C.钠离子不水解,c(Na+)=c(Na3PO4)×3;
D.根据镁和转移电子之间的关系式计算.
解答:A.甲烷的摩尔质量是16g/mol,故A错误;
B.氧气和臭氧属于同分异构体,组成元素相同,所以氧元素的摩尔质量相同,二者质量相同,所以氧原子的质量相同,根据N=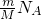 知,二者原子个数相同,故B错误;
知,二者原子个数相同,故B错误;
C.钠离子不水解,c(Na+)=c(Na3PO4)×3=0.6?mol?L-1,故C正确;
D.24?g?Mg与足量稀盐酸反应转移的电子数约为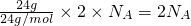 ,故D错误;
,故D错误;
故选C.
点评:本题考查摩尔质量、物质的量的有关计算,易错选项是B,根据原子质量和摩尔质量的关系计算原子个数即可,为易错点.
本题难度:困难
2、填空题 实验室欲配制90mL浓度为1.00mol?L-1的Na2CO3溶液:
(1)配制时的实验步骤为:计算、称量、溶解、转移(洗涤)、______、摇匀;
(2)某同学欲称量Na2CO3的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图.烧杯的实际质量为______g,要完成本实验该同学应称出______?g?Na2CO3.

(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)
①转移溶液时玻璃棒插在了刻度线以上的位置______;
②容量瓶不干燥,含有少量蒸馏水______.
参考答案:(1)配制实验操作顺序为:称量、溶解、冷却、移液、洗涤、定容以及摇匀等操作,故答案为:定容;
(2)左盘内质量为30g,游码的数值为2.6g,所以烧杯的实际质量为30g-2.6g=27.4g.没有90mL容量瓶,选择规格相近的容量瓶,故溶液应配制100mL,所以配制100mL1.00mol?L-1的Na2CO3溶液需要Na2CO3质量为:1.00mol/L×0.1L×106g/mol=10.6g,故答案为:27.4;10.6;
(3)①转移溶液时玻璃棒插在了刻度线以上的位置,刻度线以上有液体悬挂,定容后所配溶液体积偏大,所配溶液浓度偏低,故答案为:偏低;
②配制最后需要定容,容量瓶不干燥,含有少量蒸馏水,对所配溶液浓度无影响,故答案为:无影响.
本题解析:
本题难度:一般
3、选择题 取100mL?0.3mol/L和300mL?0.25mol/L的硫酸混合后加水配制成500mL溶液,该混合溶液中H+的物质的量浓度是
A.0.21mol/L
B.0.42mol/L
C.0.56mol/L
D.0.24mol/L
参考答案:B
本题解析:分析:先利用n=cV来计算每份硫酸溶液中硫酸的物质的量,从而计算出H+的物质的量,再利用混合后溶液的体积及c= 来计算H+的物质的量浓度.
来计算H+的物质的量浓度.
解答:100mL0.3mol/L硫酸溶液中硫酸的物质的量为0.1L×0.3mol/L=0.03mol,
300mL0.25mol/L的硫酸溶液中硫酸的物质的量为0.3L×0.25mol/L=0.075mol,
则混合后硫酸的物质的量为0.03mol+0.075mol=0.105mol,
H+的物质的量为0.105mol×2=0.21mol,
则该混合溶液中H+的物质的量浓度为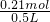 =0.42mol/L,
=0.42mol/L,
故选B.
点评:本题考查物质的量浓度的计算,明确物质的量、溶液的体积、浓度之间的关系及硫酸与氢离子的关系即可解答,难度不大.
本题难度:简单
4、填空题 掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
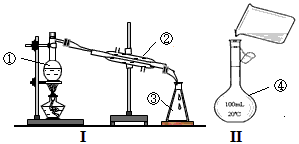
(1)写出下列仪器的名称: ①____________;②_____________; ④__________;?
(2)仪器①~④中,使用时必须检查是否漏水的有_____________。(填序号)
(3)若利用装置I分离四氯化碳和乙醇的混合物,还缺少的仪器是_________,将仪器补充完整后进行的实验操作的名称为_____________ 。
(4)现需配制250 mL 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是
______________、_________________ 。
参考答案:(1)蒸馏烧瓶;冷凝管;容量瓶
(2)④
(3)温度计;分馏;
(4)未用玻璃棒引流;未采用250ml容量瓶
本题解析:
本题难度:一般
5、简答题 实验室用胆矾(CuSO4?5H2O)配制490mL0.1mol/LCuSO4溶液,实际操作步骤有:
(1)需称量胆矾的质量为______g
(2)配制溶液时下列仪器中:
A.锥形瓶B.200mL容量瓶C.烧杯D.胶头滴管E.药匙F.托盘天平
不需要用到的是______和______(填序号),尚缺的玻璃仪器有______和______(写名称).
(3)人们常将配制过程简述为以下各步骤:A.冷却B.称量C.洗涤D.定容E.溶解F.摇匀G.转移H.装瓶.其正确的操作顺序应是______(填序号).
①BEFGCGDHA②BEGACGFDH
③BEAGCGDFH④BEAGCGDHF
(4)配制过程中,下列情况会使配制结果偏高的是______(填序号)
①定容时俯视刻度线观察液面②定容时仰视刻度线观察液面③容量瓶使用时未干燥④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线⑤移液时未洗涤烧杯和玻璃棒⑥胆矾晶体部分失水.
参考答案:(1)需要硫酸铜的物质的量等于硫酸铜晶体的物质的量,实验室没有490mL容量瓶,应选择500mL容量瓶,配制500mL0.1mol/LCuSO4溶液,需要硫酸铜晶体的质量为0.1L×0.5mol/L×250g/mol=12.5g,故答案为:12.5;
(2)配制顺序是:计算→称量→溶解、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.
所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管.
故所以不需要的仪器有:A.锥形瓶、B.200mL容量瓶.
所缺少的仪器为:玻璃棒500mL容量瓶.
故答案为:A;B;烧杯;玻璃棒;
(3)由(2)中的实验操作步骤可知,正确的存在顺序为BEAGCGDFH,故选:③;
(4)①定容时俯视刻度线观察液面,导致所配溶液的体积偏小,所配溶液的浓度偏高;
②定容时仰视刻度线观察液面,导致所配溶液的体积偏大,所配溶液的浓度偏低;
③溶液配制需加水定容,容量瓶使用时未干燥,对所配溶液浓度无影响;
④定容后经振荡、摇匀、静置,发现液面低于刻度线,少量溶液残留在瓶塞与瓶口之间,再加蒸馏水补至刻度线,导致所配溶液的体积偏大,溶液的浓度偏低;
⑤移液时未洗涤烧杯和玻璃棒,移入容量瓶内硫酸铜的质量减小,所配溶液浓度偏低;
⑥胆矾晶体部分失水,晶体中硫酸铜的含量增大,实际称取的晶体中硫酸铜的质量偏大,所配溶液浓度偏大.
故选:①⑥.
本题解析:
本题难度:简单