1、选择题 25 ℃时,在等体积的①pH=0的硫酸溶液、②0.05 mol/L的Ba(OH)2溶液、③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是(? )
A.1∶10∶1010∶109
B.1∶5∶5×109∶5×108
C.1∶20∶1010∶109
D.1∶10∶104∶109
参考答案:A
本题解析:①pH=0的硫酸溶液,溶液中c(H+)="1" mol/L,根据Kw=10-14,可求溶液中c(OH-)=1×10-14 mol/L,故由水电离出的c(H+)水=c(OH-)=1×10-14 mol/L;
②0.05 mol/L的Ba(OH)2溶液中c(OH-)=10-1 mol/L,根据Kw=10-14,可求溶液中c(H+)=1×10-13 mol/L,故c(H+)水=1×10-13 mol/L;③pH=10的Na2S溶液,溶液中c(H+)=1×10-10 mol/L,根据Kw=10-14,可求溶液中c(OH-)=1×10-4 mol/L,溶液中OH-完全来自于水的电离,故由水电离出的c(OH-)和c(H+)都是1×10-4 mol/L;④pH=5的NH4NO3溶液中c(H+)=1×10-5 mol/L,溶液中H+完全来自于水的电离,故由水电离出的H+是1×10-5 mol/L;综上所述:①中c(H+)水=1×10-14 mol/L,②中c(H+)水=1×10-13 mol/L,③中c(H+)水=1×10-4 mol/L,④中c(H+)水=
1×10-5 mol/L,求比值可得1∶10∶1010∶109,即A项正确。
本题难度:一般
2、选择题 下列物质加入水中,能使水的电离程度增大,且所得溶液显酸性的是(?)
A.CH3COOH
B.Al2(SO4)3
C.NaOH
D.Na2CO3
参考答案:B
本题解析:影响水的电离平衡的外界条件有:温度、溶液酸碱性、盐类水解等。将CH3COOH加入水中,则增大水中的[H+],从而会抑制水的电离,减小了的电离程度,但是由于CH3COOH的电离,溶液呈酸性。NaOH的加入,则增大水中的[OH-],从而会抑制水的电离,减小了水的电离程度,溶液呈碱性。B、D都是盐类,并且一个是强酸弱碱盐,一个是强碱弱酸盐,把它们加入到水中,都会发生水解,结合水电离产生的OH-和H+,使平衡向电离的方向移动,从而会促进水的电离。
本题难度:简单
3、选择题 在25℃时,向50.00 mL未知浓度的CH3COOH溶液中逐滴加入0.5 mol・L-1的NaOH溶液。滴定过程中,溶液的pH与滴入NaOH溶液体积的关系如图所示,则下列说法中,正确的是
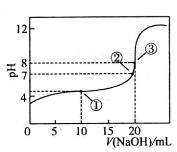
A.该中和滴定过程,最宜用石蕊作指示剂
B.图中点②所示溶液中,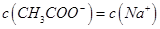
C.图中点①所示溶液中水的电离程度大于点③所示溶液中水的电离程度
D.滴定过程中的某点,会有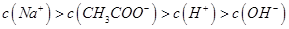 的关系存在
的关系存在
参考答案:B
本题解析:A、石蕊颜色变化不明显,不能用作酸碱中和滴定的指示剂,错误;B、图中点②pH=7,根据溶液呈中性,可得c(H+)+c(Na+)=c(CH3COO?)+c(OH?),可得c(CH3COO?)=c(Na+),正确;C、图中点①pH为4,H+浓度为10-4mol?L?1,抑制了水的电离,点③pH=8,OH?浓度为10-6mol?L?1,抑制水的电离作用较弱,所以图中点①所示溶液中水的电离程度小于点③所示溶液中水的 www.91exAm.org电离程度,错误;D、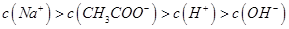 违背了电荷守恒,错误。
违背了电荷守恒,错误。
本题难度:一般
4、选择题 25℃时,由弱酸(HA)及其盐(NaA)组成的混合溶液,起始浓度均为1mol・L-1。下图为向该溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入H+或OH-的物质的量而变化的曲线。下列说法中,不正确的是
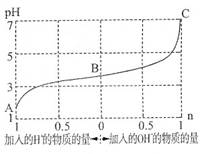
A.A、B、C三点所表示的溶液中水的电离程度依次增大
B.通入HCl,HA的电离常数减小,A-的水解程度增大
C.加入1 mol NaOH后,溶液中c(Na+)=c(A-)
D.未加HCl和NaOH时,溶液中c(A-)>c(Na+)>c(HA)
参考答案:B
本题解析:A、A点H+浓度最大,对水的电离程度抑制作用最强,C点pH=7,对水的电离程度无抑制作用,所以A、B、C三点所表示的溶液中水的电离程度依次增大,正确;B、温度不变,HA的电离常数不变,错误;C、根据图像,加入1 mol NaOH后,溶液的pH=7,则c(H+)=c(OH?),根据电荷守恒可得c(H+)+c(Na+)=c(OH?)+c(A-),所以c(Na+)=c(A-),正确;D、未加HCl和NaOH时,溶质为HA和NaA,有图像可知pH<7,溶液显酸性,HA的电离程度大于NaA的水解程度,所以c(A-)>c(Na+)>c(HA),正确。
本题难度:一般
5、选择题 常温下pH=6的盐酸和pH=6的NH4Cl溶液,其中由水电离出的c(H+)分别为x mol/L、y mol/L,则x与y的关系是(? )
A.x=10-2y
B.x >y
C.x=y
D.x=102y
参考答案:A
本题解析:常温下pH=6的盐酸,c(H+)(酸)=10-6mol/L,c(OH-)=Kw÷c(H+)(酸)=10-8mol/L. c(H+)(水)= c(OH-)=10-8mol/L。pH=6的NH4Cl溶液,c(H+)(水)=10-6mol/L。所以x:y=10-8mol/L: 10-6mol/L=1:100.因此正确选项为A。
本题难度:一般