1、填空题 (1)分别写出由钠在一定条件下生成下列物质的化学方程式(必须注明反应条件)。
①Na2O2:________;
②Na2O:________。
(2)指出氧在下列各物质中的化合价。O3:__;Na2O2:___;Na2O:___.
(3) KO2能吸收CO2生成K2CO3和O2,故可用作特殊情况下的氧气源,试写出该反应的化学方程式___。
参考答案:(1)①2Na+O2 Na2O2
Na2O2
②4Na+O2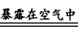 2Na2O
2Na2O
(2)0价 ;-1价 ;-2价
(3)4KO2+2CO2= 2K2CO3+3O2
本题解析:
本题难度:一般
2、选择题 取16.8g碳酸氢钠固体,加热一段时间后,剩余固体的质量为13.7g。把剩余固体加入到100mL 2mol/L的稀硫酸中,充分反应后溶液中H+的浓度约为
A.3 mol/L
B.2 mol/L
C.1.4 mol/L
D.1 mol/L
参考答案:B
本题解析:根据反应结果分析,无论碳酸氢钠还是分解后的碳酸钠,钠原子量不变,根据产物硫酸钠得出反应的硫酸的量为钠原子量的一半(Na2SO4),故剩余硫酸的量为:0.1×2-16.8÷84÷2=0.1mol,反应后H+的浓度约为0.1mol×2÷0.1L="2" mol/L。
本题难度:一般
3、选择题 下列关于钠的氧化物的叙述正确的是
A.Na2O2是白色固体,和?冷水作用得到O2和NaOH
B.Na2O2与水的反应中,氧化剂是Na2O2,还原剂是水
C.Na2O不稳定,能继续被O2氧化生成Na2O2
D.都能与酸反应,生成含氧酸盐,都是碱性氧化物
参考答案:C
本题解析:A.不正确,Na2O2是淡黄色固体; B.不正确,Na2O2与水的反应中,氧化剂是Na2O2,还原剂也是Na2O2; C.正确; D.不正确,都能与酸反应,不一定生成含氧酸盐,Na2O是碱性氧化物,Na2O2不是。选C。
本题难度:简单
4、填空题 (12分)在两份体积相同的NaOH溶液中,分别通入CO2气体,充分反应后,在所得溶液A、B中分别加入1mol/L的盐酸,所加盐酸体积(mL)与产生CO2气体的体积(L)的关系如图所示,试填写下列空白:

⑴两份NaOH溶液A和B的物质的量浓度之比为?,通入CO2气体的体积之比是(相同条件)?。
⑵与盐酸反应前,A溶液中的溶质是?,其物质的量之比是?。
⑶与盐酸反应前,B溶液中的溶质是?,其物质的量之比是?。
参考答案:
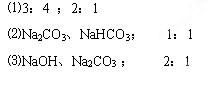
本题解析:略
本题难度:一般
5、选择题 为维持人体体液平衡,人在大量出汗后应及时补充的离子是(?)
A.Mg2+
B.Ca2+
C.Na+
D.Fe3+
参考答案:C
本题解析:大量出汗后,钠元素以氯化钠的形式在汗液中被排出体外,因此要及时补充Na+,Ca、Fe、Mg等也是人体所需的重要元素,但不一定要在大量出汗后及时补充。
本题难度:简单