1��ѡ���� ������������ķ�����һ����ȵ���
A.������ȣ��ܶȲ��ȵ�N2��C2H4
B.���ܶȡ�������ȵ�CO2��C2H4
C.���µ������O2��N2
D.��ѹ�������N2��CO2
�ο��𰸣�A
�����������������������ʵ�����ͬ���еķ�����һ����ͬ��
A��N2��C2H4��Ħ����������28g/mol������������ʵ�����ȣ�
B�����ܶȡ�������ȵ�CO2��C2H4��������������ȣ����ߵ�Ħ����������ȣ����ʵ����������Ҳ���ܲ���ȣ�
C�����µ����Ӱ����������ʵ���������ѹǿ�������ѹǿ��һ����ͬ��
D����ѹ�����Ӱ����������ʵ����������¶ȣ�������¶������ʵ����ɷ��ȣ�
���A��N2��C2H4��Ħ����������28g/mol����������������ʵ�����ȣ�����������һ����ȣ���A��ȷ��
B�����ܶȡ�������ȵ�CO2��C2H4��������������ȣ����ߵ�Ħ����������ȣ����ʵ����������Ҳ���ܲ���ȣ������ķ������������Ҳ���ܲ���ȣ���B����
C�����µ������O2��N2�����ߵ�ѹǿ��һ����ͬ����ѹǿ��ͬ�����еķ�������ͬ����ѹǿ��ͬ���еķ�������ͬ����C����
D����ѹ�������N2��CO2�����ߵ��¶Ȳ�һ����ͬ�����¶���ͬ�����еķ�������ͬ�����¶Ȳ�ͬ�����еķ��������¶ȳɷ��ȣ���D����
��ѡ��A��
���������鰢��٤�����ɼ����ۣ��ѶȲ����Խ���pV=nRT���Ⱒ��٤�����ɼ����ۣ�
�����Ѷȣ�һ��
2��ѡ���� �谢���ӵ�������ֵΪNA������˵������ȷ����?
[? ]
A��1mol����ϩ�к��е�C��C��Ϊ4NA
B��2.8?g��ϩ�ͱ�ϩ�Ļ������������̼ԭ����Ϊ0.2NA
C��0.1molCnH2n+2�к��е�C��C����Ϊ0.1nNA
D����״���£�2.24LCHCl3���еķ�����Ϊ0.1NA
�ο��𰸣�B
���������
�����Ѷȣ���
3��ѡ���� ��NA��ʾ�����ӵ�������������������ȷ���ǣ�������
A�����ʵ���Ũ��Ϊ0.5mol/LMgCl2��Һ��������������Ϊ1NA
B��64gSO2������ԭ����Ϊ1NA
C����״���£�22.4LH2O�ķ�����Ϊ1NA
D�����³�ѹ�£�14gN2���з�����Ϊ0.5NA
�ο��𰸣�A����Һ�����δ֪��������������������A����
B��n��SO2��=mM=64g64g/mol=1mol��ÿ��SO2�����к���2����ԭ�ӣ�������ԭ�ӵ����ʵ���Ϊ2mol����ԭ����Ϊ2 NA����B����
C������Ħ�����Vm=22.4L/mol��ʹ�÷�ΧΪ��һ������ܹ���Ļ�����壨����£��������ˮΪҺ�壬���Բ���ʹ������Ħ���������C����
D��n��N2��=mM=14g38g/mol=0.5mol������14gN2���еķ�����Ϊ0.5mol��NAmol-1=0.5NA ����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
4��ѡ���� ��NA���������ӵ���������ֵ������˵����ȷ����
[? ]
A����״���£�11.2L�ȷ£�CHCl3���к���C-Cl������ĿΪ1.5NA
B��0.05mol���ڵ�KHSO4�к��������ӵ���ĿΪ0.05 NA
C��500�桢30MPa�£�N2��g��+3H2��g��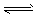 2NH3��g������H=-38.6kJ/mol����1.5NA��H2����N2�ڴ������³�ַ�Ӧ���ų�����19.3kJ
2NH3��g������H=-38.6kJ/mol����1.5NA��H2����N2�ڴ������³�ַ�Ӧ���ų�����19.3kJ
D�����³�ѹ�£�17g����-14CH3��������������Ϊ9NA
�ο��𰸣�D
���������
�����Ѷȣ���
5��ѡ���� ��NAΪ����٤����������ֵ������˵����ȷ����
A.�����ʵ�����CH4��CO������������ΪNA
B.1?mol?FeCl3�Ƴɽ��壬���ý���������ĿΪNA
C.�����£�34.5g?NO2��N2O4�Ļ�����к���1.5NA����ԭ��
D.��KClO3+6HCl�TKCl+3Cl2��+3H2O�У�ÿ����3molCl2ת�Ƶ�����Ϊ6NA
�ο��𰸣�C
���������������A�������ʵ�����һ����1mol��
B���������������������ļ����壻
C������NO2��N2O4���ʽ��ͬ��ֻ��Ҫ����34.5gNO2����ԭ�����ʵ�����
D������������ԭ��Ӧ����ʽ��Ԫ�ػ��ϼ۱仯�������ת�ƣ�
���A�������ʵ�����CH4��CO������������ͬ����һ����ΪNA����A����
B��1 mol FeCl3�Ƴɽ��壬�����������������ļ����壬���ý���������ĿС��NA����B����
C�������£�NO2��N2O4���ʽ��ͬ��ֻ��Ҫ����34.5gNO2����ԭ�����ʵ���= ��2=1.5mol��34.5g NO2��N2O4�Ļ�����к���1.5NA����ԭ�ӣ���C��ȷ��
��2=1.5mol��34.5g NO2��N2O4�Ļ�����к���1.5NA����ԭ�ӣ���C��ȷ��
D����KClO3+6HCl�TKCl+3Cl2��+3H2O�У�ÿ����3molCl2��1molKClO3��Cl2��5e-��ת�Ƶ���5mol��5molHCl��Cl2��5e-������ת����Ϊ5NA����D����
��ѡC��
���������⿼���˰���٤��������Ӧ�ã���Ҫ�ǽ������ӵ� ��������������������ʵ�������������������ԭ��Ӧ�ĵ���ת�Ƽ���Ӧ�ã���Ŀ�Ѷ��еȣ�
�����Ѷȣ���