1、选择题 将淀粉与KI的混合液装在半透膜中,浸泡在盛有蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行实验,能证明半透膜有破损的是
A.加入碘水不变蓝色
B.加入碘水变蓝色
C.加入AgNO3溶液不产生黄色沉淀
D.加入AgNO3溶液产生黄色沉淀
参考答案:B
本题解析:由于胶体不能透过半透膜,而溶液是可以的。所以如果半透膜有破损,则淀粉一定难透过半透膜,烧杯中液体中一定含有淀粉,碘和淀粉能发生显色反应,据此可以检验,答案选B。
本题难度:一般
2、填空题 (12分)纳米ZnS具有独特的光电效应,在电学、磁学、光学等领域应用广泛。以工业废渣锌灰(主要成分为Zn、ZnO,还含有Fe2O3、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:
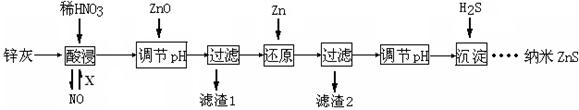
请回答下列问题。
(1)酸浸时FeO与稀HNO3反应的离子方程式?。
(2)将酸浸的尾气循环利用,加入的X气体可以是?。
(3)流程中加入ZnO调pH的目的是?。
(4)滤渣2中的成分是?。
(5)已知ZnS的溶度积Ksp=1.6×10-24,溶液中Zn2+浓度为0.01mol・L-1,则溶液中S2―浓度大于?mol・L一1,才生成ZnS沉淀。
(6)试设计简单实验方案,判断所得ZnS样品颗粒是否为纳米级???。
参考答案:(1)3FeO+10H++NO3―=3Fe3++NO+5H2O?(2分)
(2)空气(或O2)?(2分)
(3)除去溶液中的Fe3+?(2分)
(4)Cu、Zn?(2分)
(5)1.6×10―22?(2分)
(6)取少量样品和水混合形成分散系,让一束光照射,若出现一条光亮的通路,则是纳米级,否则不是。?(2分)
本题解析:(1)HNO3把FeO氧化为Fe3+,HNO3被还原为NO,配平可得离子方程式:3FeO+10H++NO3―=3Fe3++NO+5H2O
(2)NO与O2、H2O反应可生成HNO3,实现尾气循环利用,所以X气体为空气(或O2)。
(3)加入硝酸后,与Fe2O3、FeO反应生成Fe3+,流程中加入ZnO调pH可使Fe3+转化为Fe(OH)3沉淀,所以加入ZnO调pH的目的是除去溶液中的Fe3+?
(4)加入Zn后,Zn与Cu2+反应生成Cu,所以滤渣2中的成分是Cu、Zn
(5)c(S2?)= Ksp÷c(Zn2+)=1.6×10-24÷0.01=1.6×10―22mol?L?1,所以溶液中S2―浓度大于1.6×10―22mol?L?1,才生成ZnS沉淀。
(6)纳米级颗粒与水混合可形成胶体,具有丁达尔效应,所以实验方案为:取少量样品和水混合形成分散系,让一束光照射,若出现一条光亮的通路,则是纳米级,否则不是。sp的计算。
本题难度:一般
3、选择题 下列说法正确的是
A.胶体粒子的直径很小可以透过滤纸,因此可以用过滤的方法分离胶体和溶液
B.布朗运动不是胶体特有的性质
C.直径介于l-100nm之间的微粒称为胶体
D.有的胶体带正电荷或者负电荷,在电压作用下可电泳
参考答案:B
本题解析:略
本题难度:一般
4、选择题 悬浊液、乳浊液、溶液和胶体都是(? )?
A.稳定的液体
B.透明的液体
C.混合物
D.化合物
参考答案:C
本题解析:分散系均是由分散质与分散剂组成的混合物,但它们的稳定性及状态不同。
本题难度:简单
5、选择题 下列说法正确的是
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,,即布朗运动
D.电解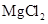 饱和溶液,可制得金属镁
饱和溶液,可制得金属镁
参考答案:A
本题解析:A.明矾中的铝离子水解生成氢氧化铝胶体,具有吸附悬浮杂质的作用;可用于水的净化;故①正确;B.通电时,溶液中的带有电荷的粒子都会分别向两极移动,错误;C.溶液中溶质粒子的也无运动规律,错误;D.由于氢离子放电优于镁离子,故在水溶液中不能得到金属镁,错误;
本题难度:一般