1、选择题 一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g) C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是(?)
C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是(?)
①混合气体的密度不再变化时?②容器内气体的压强不再变化时
③混合气体的总物质的量不再变化时?④ B物质的量浓度不再变化时
⑤当V正(C) = V逆(D) 时?⑥当V正(B) = 2V逆(C)
A.①④⑤⑥? B.②③⑥? C.②④⑤⑥? D.只有④
参考答案:A
本题解析:该反应是个体积不变的反应,②③不是平衡状态的标志。由于总的质量随着A的改变而改变,V不变,密度是平衡状态的标志。①④⑤⑥都是平衡状态的标志。
本题难度:一般
2、选择题 下列说法错误的是?(?)
A.由于合成氨反应△H<0,△S>0,所以该反应能自发进行
B.将pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸所需加入的水多
C.溴水中有下列平衡:Br2+H2O HBr+HBrO,当加入AgNO3溶液后溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后溶液颜色变浅
D.弱电解质在溶液中达到电离平衡后,加水稀释,平衡向电离的方向移动
参考答案:AB
本题解析:A错,由自由能变△G=△H―T△S<0反应一定能自发,但合成氨的反应为△S<0的反应。B错,醋酸为弱酸加水稀释会不断电离出氢离子,所以,将pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水多。C正确,当加入AgNO3溶液能破坏:Br2+H2O HBr+HBrO平衡,使平衡向右移动,溶液中溴的浓度减少,颜色变浅;D正确,弱电解质的电离为越稀越易电离,电离程度越大;
HBr+HBrO平衡,使平衡向右移动,溶液中溴的浓度减少,颜色变浅;D正确,弱电解质的电离为越稀越易电离,电离程度越大;
本题难度:一般
3、选择题 在一定温度下将1mol CO和9mol水蒸气放在密闭的容器中发生下列反应:
CO(g)+H2O(g) CO2(g)+H2(g)达到平衡后,已知该反应平衡常数为K=1.0,达到新的平衡后,CO2和H2的物质的量之和为(?)
CO2(g)+H2(g)达到平衡后,已知该反应平衡常数为K=1.0,达到新的平衡后,CO2和H2的物质的量之和为(?)
A.1.2mol
B.1.5mol
C.1.8mol
D.2.5mol
参考答案:C
本题解析:考查可逆反应的有关计算,一般采用三段式。
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始量(mol)? 1? 9? 0? 0
转化量(mol)? x? x? x? x
平衡量(mol)? 1-x? 9-x? x? x
所以有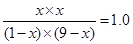
解得x=9/10
所以CO2和H2的物质的量之和为x+x=1.8mol,答案选C。
本题难度:一般
4、选择题 在一定温度下将1mol CO和3mol水蒸气放在密闭的容器中发生下列反应:
CO(g)+H2O(g)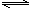 CO2(g)+H2(g)
CO2(g)+H2(g)
达到平衡后,测得 CO2为0.75mol,再通入6mol水蒸气,达到新的平衡后,CO2和H2的物质的量之和为
[? ]
A.1.2mol
B.1.5mol
C.1.8mol
D.2.5mol
参考答案:C
本题解析:
本题难度:一般
5、填空题 (19分)高炉炼铁中发生的基本反应之一如下:FeO(s)+ CO (g)  ?Fe(s)+ CO2(g)?△H>0
?Fe(s)+ CO2(g)?△H>0
(1)此反应的平衡常数表达式为:K=?;
(2)温度升高,达到新的平衡后,高炉内CO2与CO的体积比?(填“增大”、 “减小”或“不变”。);
(3)已知1100℃时,K= 0.263。某时刻测得高炉中c(CO2)= 0.025mol/L,c(CO)= 0.1mol/L,在这种情况下,该反应?(填“是”或“不是”)处于化学平衡状态。
如果“不是”,此时化学反应向?方向进行(填“正反应”或“逆反应”)。如果“是”,此空不填。
(4)在一定温度下,10L密闭容器中加入5molSO2、4.5molO2,发生反应2SO2+O2 2SO3经10min后反应达平衡时有3molSO3生成。试计算:
2SO3经10min后反应达平衡时有3molSO3生成。试计算:
①O2的转化率为:?
②平衡常数K为:?
参考答案:

本题解析:略
本题难度:简单