1、选择题 由反应:①Tl3++2Ag→Tl++2Ag+;②Fe+Cu2+→Fe2++Cu;③2Ag++Cu→Cu2++2Ag 得出的结论正确的是
A.氧化性:Ag+>Tl3+>Cu2+>Fe2+
B.还原性: Fe>Cu>Ag>Tl
C.氧化性:Tl 3+>Ag+>Cu 2+>Fe 2+
D.还原性: Tl +>Ag>Cu>Fe
参考答案:C
本题解析:①Tl3++2Ag→Tl++2Ag+;氧化剂Tl3+氧化性大于氧化产物Ag+;还原剂Ag还原性大于还原产物Tl+;②Fe+Cu2+→Fe2++Cu; 氧化剂Cu2+氧化性大于氧化产物Fe2+;还原剂Fe还原性大于还原产物Cu;③2Ag++Cu→Cu2++2Ag 氧化剂Ag+氧化性大于氧化产物Cu2+;还原剂Cu还原性大于还原产物Ag;得到氧化性顺序:Tl3+>Ag+>Cu2+>Fe2+;还原性顺序Fe>Cu>Ag>Tl+;故选C。
本题难度:一般
2、填空题 (14分)NaClO具有强氧化性,其溶液可用于游泳池及环境消毒。
(1)已知:
①Cl2(g)+2NaOH(aq)=NaCl(aq)+NaClO(aq)+H2O(l) △H=-101.1kJ・mol-1
②3NaClO(aq)=2NaCl(aq)+NaClO3(aq) △H=-112.2kJ・mol-1
则3Cl2(g)+6NaOH(aq)=5NaCl(aq)+NaClO3(aq)+3H2O(l) △H=
( 2)工业上可用石墨电极电解饱和氯化钠溶液制取次氯酸钠溶液装置如图所示

①电源中,a电极名称是
②用此装置电解热的氯化钠溶液时会有部分氯酸钠生成,若电解消耗了117g氯化钠时,电路中共转移的电子为8mol,则次氯酸钠的产率为
(3)向次氯酸钠溶液通入少量的CO2,只生成次氯酸钠和碳酸氢钠,则相同温度下,等物质的量浓度的Na2CO3、NaClO、NaHCO3溶液的pH由大到小的顺序为 。
(4)向盛有硫酸酸化的淀粉KI溶液的试管中,滴加少量次氯酸钠溶液,会立即观察到溶液变成蓝色,该反应的离子方程式为 。再向上述的蓝色溶液中,继续滴加Na2SO3溶液,又发现蓝色溶液逐渐褪色,该反应的化学方程式为 。对比上述两组实验所得结果,比较ClO
参考答案:
本题解析:
本题难度:困难
3、选择题 下列实验中,依据实验操作及现象,得出的结论正确的是
| 操作
| 现象
| 结论
|
A
| 将水蒸气通过灼热的铁粉
| 粉末变红
| 铁与水在高温下发生反应
|
B
| 将充满NO2的密闭玻璃球浸泡在热水中
| 红棕色变深
| 反应2NO2(g) N2O4(g);ΔH<0 N2O4(g);ΔH<0
|
C
| 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡
| 上层分别呈无色和紫红色
| 还原性:I->Br->Fe2+
|
D
| 向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中
| 生成白色沉淀
| 溶液X中一定含有CO32-或SO32-
|
参考答案:B
本题解析:A、铁与水蒸气反应生成黑色的四氧化三铁,错误;B、红棕色变深,说明升高温度,平衡逆向移动,则正向是放热反应,正确;C、因为溴水是少量的,所以溴先与碘离子反应生成碘单质,而溴是否与亚铁离子反应,无法判断,所以不能比较亚铁离子和溴离子的还原性,错误;D、产生使澄清石灰水变浑浊的气体的离子除碳酸根离子、亚硫酸根离子外,还有亚硫酸氢根离子、碳酸氢根离子,所以不能确定溶液中一定存在碳酸根离子或亚硫酸根离子,错误,答案选B。
考点:考查物质的化学性质,离子的判断
本题难度:一般
4、选择题 在反应 3S + 6NaOH 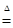 2Na2S + Na2SO3 + 3H2O 中被氧化的硫与被还原的硫的关系是 ( )
2Na2S + Na2SO3 + 3H2O 中被氧化的硫与被还原的硫的关系是 ( )
A.物质的量之比为2∶1
B.质量比为2∶1
C.质量比为 1∶2
D.物质的量之比为1∶1