1、选择题 对于复分解反应:X+Y=Z+W,下列叙述正确的是?(?)
A.若Z是强酸,则X或Y必有一种是酸
B.若Y是强碱,X是盐,则Z或W必有一种是弱碱
C.若W是弱碱,Z是盐,则X或Y必有一种是强碱
D.若X是强酸,Y是盐,反应后可能有强酸或弱酸生成
2、选择题 下列有关实验操作 、现象和解释或结论都正确的是
、现象和解释或结论都正确的是
?
| 操作
| 现象
| 结论
|
A
| 向Na2CO3稀溶液中通入足量CO2?
| 溶液变浑浊
| 析出了NaHCO3
|
B
| 向无色溶液中滴加氯水和CCl4,振荡、静置
| 下层溶液显紫色
| 原溶液中有I-
|
C
| Al箔插入稀HNO3中
| 无现象
| Al箔---表面被HNO3氧化,形成致密的氧化膜
|
D
| 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液
| 溶液呈红色
| 稀HNO3将Fe氧化为Fe3+
3、选择题 核反应中会产生I-131,而我们生活中常见的是含I-127的碘及碘的化合物,下列说法正确的是?
[? ]
A.I-131和I-127互为同位素 ?
B.食盐中含碘的物质是碘化钾 ?
C.分离氯化钠和碘单质可以用过滤的方法 ?
D.I-131和I-127化学性质不同
4、选择题 几种短周期元素的原子半径及主要化合价如下表
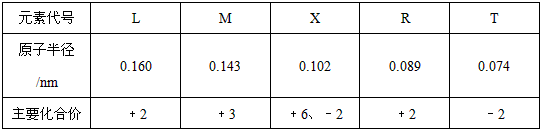
下列叙述正确的是
[? ]
A.离子半径大小:r(M3+)>r(T2-)
B.R的氧化物对应的水化物可能具有两性
C.X单质可在氧气中燃烧生成XO3
D.L、X形成的简单离子核外电子数相等
5、填空题 金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3.5%(质量分数)
CaO。
(1)Ca元素在周期表中位置是___________,其原子结构示意图___________。
(2)Ca与最活跃的非金属元素A形成化合物D,D的电子式为___________,D的沸点比A与Si形成的化合物E的沸点___________。
(3)配平用钙线氧脱鳞的化学方程式
____P+_____FeO+_____CaO ______ ______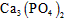 +_____Fe +_____Fe
(4)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色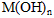 ,则金属M为__________;检测的方法是____________________(用离子方程式表达)。 ,则金属M为__________;检测的方法是____________________(用离子方程式表达)。
(5)取1.6g钙线试样,与水充分反映,生成224ml H2(标准状况),在向溶液中通入适量的CO2,最多能得到CaCO3___________g。
|