1��ѡ���� �������У����ԭ�Ӿ�����ͬ���Ӳ�ṹ���ǣ�������
A��Na+
B��
C��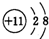
D��Ne
�ο��𰸣�A��Na+���ӽṹʾ��ͼΪ�� �������Ӻ�����10�����ӣ���Neԭ�ӵ��Ӳ�ṹ��ͬ����A����
�������Ӻ�����10�����ӣ���Neԭ�ӵ��Ӳ�ṹ��ͬ����A����
B�������ӽṹʾ��ͼΪ��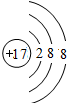 ��������18�����ӣ���벵ĵ��Ӳ�ṹ��ͬ����B��ȷ��
��������18�����ӣ���벵ĵ��Ӳ�ṹ��ͬ����B��ȷ��
C��Na+���ӽṹʾ��ͼΪ�� �����Ը�ʾ��ͼΪ�����ӣ�������10���ӣ���Neԭ�ӵ��Ӳ�ṹ��ͬ����C����
�����Ը�ʾ��ͼΪ�����ӣ�������10���ӣ���Neԭ�ӵ��Ӳ�ṹ��ͬ����C����
D��Neԭ�Ӻ�����10�����ӣ���D����
��ѡB��
���������
�����Ѷȣ���
2��ѡ���� �����й�Ԫ�����ʵ�˵������ȷ���ǣ�������
A���������е���ʽ��ԭ���У���1s22s22p63s23p2��1s22s22p3��1s22s22p2��1s222s2p63s23p4ԭ�Ӱ뾶�����Ǣ�
B������ԭ�ӵļ۵����Ų��У���3s23p1��3s23p2��3s23p3��3s23p4��Ӧ�ĵ�һ����������Ǣ�
C����Na��K��Rb��N��P��As��O��S��Se��Na��P��ClԪ�صĵ縺����ԭ������������������Ǣ�
D��ijԪ�ص������ֱܷ�Ϊ738��1451��7733��10540��13630��17995��21703��������������Ӧʱ�������ɵ���������X3+
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3������� ��֪Ԫ�����ڱ��й���18���У���ͼʵ�߱�ʾԪ�����ڱ��ı߽磬�������Ų����ɰ����ڱ�����Ϊs����p����d����ds���ȣ���ds���⣬�����������ƾ�������ԭ�����������ӵ��ܼ�������������
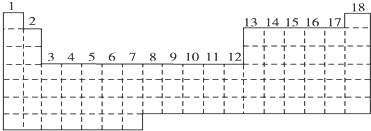
��1������ͼ����ʵ����s����p����d����ds���ı߽��ߣ�����Ƿ���______��
��2���е�ͬѧ�����ֻ��ֵ���ʾ����Ϊd����6��7���еIJ���Ԫ�ؿ���������һ��������ΪӦ����______����
��3������Ԫ�����ڱ��б��4s����������Ԫ�أ���Ԫ�ط��ű�ʾ����
��4�����ſ�ѧ�����ķ�չ���������µ�Ԫ�ر����֣����ѵ���������������Ԫ�����ڱ��������Ų�______��Ԫ�أ�
��5�������ڱ��У��縺������Ԫ����______����Ԫ�ص�ԭ�ӹ��ͼ______��д���õ�����ˮ��Ӧ�Ļ�ѧ����ʽ��______��
�ο��𰸣���1����A����A��������s���ӣ�Ϊs������A������Ϊp�����ڢ�B������B��͵ڢ���Ϊd������B�͢�B��Ϊds������ͼ��ʾΪ
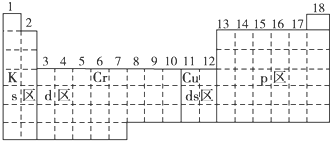
��
�ʴ�Ϊ��

��
��2������6��7���еIJ���Ԫ�أ�d���������s���Ӱ�����ȫ����Ϊ�ȶ��ṹ����ds��Ԫ�ص��ȶ��ṹ���ƣ����������ds�����ʴ�Ϊ��ds��
��3��Cr����Χ�����Ų�Ϊ3d54s1��Ϊ4s����������Cu����Χ�����Ų�Ϊ3d104s1��Ϊ4s��������������4s���������ΪCr��Cu��λ�ü���1���д𰸣�
�ʴ�Ϊ��

��
��4����һ������2��Ԫ�أ��ڶ��������ڸ���8��Ԫ�أ����ġ������ڸ���18��Ԫ�أ�������������������Ϊ32�֣�������ʱԪ�ع���2+8+8+18+18+32+32=118�֣�
�ʴ�Ϊ��118��
��5�����ڱ���F�ĵ縺�����F��ԭ�ӹ��ͼΪ

������ˮ��Ӧ����HF���������÷�ӦΪ2F2+2H2O�T4HF+O2��
�ʴ�Ϊ��F��

��2F2+2H2O�T4HF+O2��
���������
�����Ѷȣ�һ��
4��ѡ���� ����������ȷ���ǣ�������
A��H2��12H�ĺ����������ͬ
B��Cl��Cl-������Ӳ�����ͬ
C����CS2��PCl3�и�ԭ���������ܴﵽ8���ӵ��ȶ��ṹ
D��Arԭ�ӵĽṹʾ��ͼΪ��
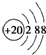
�ο��𰸣�A��H2�Ƿ��ӣ������2�����ӣ�12H��ԭ�ӣ�����ֻ��1�����ӣ���A����
B��Cl��Cl-����3�����Ӳ㣬��B����
C���жϴ�8���ӵķ�����ԭ������������+���ϼ۵ľ���ֵ=8�ʹ�8���ӣ������ǣ��������������ж�֪��CS2��PCl3�и�ԭ���������ܴﵽ8���ӵ��ȶ��ṹ����C��ȷ��
D��Arԭ�ӵĽṹʾ��ͼӦΪ
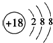
����D����
��ѡC��
���������
�����Ѷȣ�һ��
5������� ��1����̬��ԭ�ӵļ۵����Ų�ʽ��______�����������к���һ��______��������______����
��2�������ӵĿռ乹��Ϊ______������1���Ӱ����е�����P-P����������һ����ԭ�ӣ����ɽ��______����ԭ�ӣ���ÿ��Pԭ���ϵŶԵ��ӷֱ�������λ������һ����ԭ�ӣ��Ϳ��Եõ�����һ��������______�������ʽ����
��3�����ʯ�ľ���ṹ��ÿ��̼ԭ������Χ��4��̼ԭ���γ��ĸ�̼̼��������5��̼ԭ���γɵ���______�ṹ�����ʯ������Cԭ������C-C����֮��Ϊ______����������С�Ļ��ϵ�̼ԭ����Ϊ______��
�ο��𰸣���1��Nԭ�ӵ�ԭ������Ϊ6����̬��ԭ�ӵļ۵����Ų�ʽ��1s22s22p3�������ĽṹʽΪN��N������1���ļ���2���м���
�ʴ�Ϊ��1s22s22p3���ģ��У�
��2������Ϊ��������ṹ������6�����ۼ�������1���Ӱ����е�����P-P����������һ����ԭ�ӣ����ɽ��6��Oԭ�ӣ���ÿ��Pԭ���ϵŶԵ��ӷֱ�������λ������һ����ԭ�ӣ����ɽ��4��Oԭ�ӣ�����γɻ�����P4O10��
�ʴ�Ϊ���������壻6��P4O10��
��3�����ʯ������ÿ��Cԭ�Ӵ�������4��Cԭ�ӹ��ɵ�����������ڲ�������Χ���������γɿռ�������״�ṹ����С�Ļ���������Ԫ����ÿ��Cԭ����Χ��4�����ۼ�����ÿ2��̼ԭ���γ�1�����ۼ�������ʯ������Cԭ������C-C����֮��Ϊ1��2��
�ʴ�Ϊ���������壻1��2��6��
���������
�����Ѷȣ�һ��