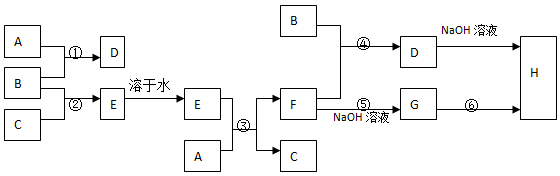
1������� ��10�֣������£�����A��B��C�ֱ�Ϊ���塢����ɫ���塢��ɫ���壬�ں��ʵķ�Ӧ�����£����ǰ�ͼ���з�Ӧ����֪E��Һ����ɫ�ģ�H�Ǻ��ɫ�������ش�
(1)A?��? B��?��?
C��?��? G��?�����ѧʽ��
(2)д���ٵĻ�ѧ��Ӧ����ʽ______________________________________________________
(3) д���ۢܵ����ӷ�Ӧ����ʽ��_____________________________________________________
��________________________________________________________
�ο��𰸣�(1) Fe? Cl2? H2?Fe(OH)2? (2)? 2Fe+3Cl2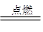 2FeCl3
2FeCl3
(3) ��Fe+2H+ =H2��+Fe2+?��2Fe2+ +Cl2 = 2Cl--+ 2Fe3+
�������������ɫ��������������B�����������ɫ��������������������H���������������ݿ�ͼ��ת���ɵó�D���������ӣ�F�к����������ӣ�����G���������������������Ϸ�����֪A�ǹ�������D���Ȼ�����E���Ȼ��⣬C��������F���Ȼ�������
�����Ѷȣ�һ��
2������� ��ͼ��ʾA--E���ֺ��������ת���Ĺ�ϵͼ������A��B��C��D�����¶������壬BΪ����ɫ��д��������Ӧ�Ļ�ѧ����ʽ��
��______
��______
��______
��______��
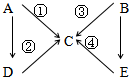
�ο��𰸣�BΪ����ɫ��ӦΪNO2������NO2�����ʿ�֪NO2��Ӧ�ֱܷ�����NO��HNO3����CӦΪNO��EΪHNO3��NO2����ˮ��Ӧ����
NO��ϡHNO3����Cu��Ӧ����NO����NԪ��������������NO�Ļ���N2��NH3������N2��������Ӧ��������NH3��
��ֱ��ǣ�A��N2��B��NO2��C��NO��D��NH3��E��HNO3��
��Ӧ�ٵķ���ʽΪN2+O2�ŵ�.2NO��
��Ӧ�ڵķ���ʽΪ4NH3+5O2����.���¸�ѹ4NO+6H2O��
��Ӧ�۵ķ���ʽΪ3NO2+H2O=2HNO3+NO��
��Ӧ�ܵķ���ʽΪ8HNO3+3Cu=3Cu��NO3��2+2NO+4H2O��
�ʴ�Ϊ��N2+O2�ŵ�.2NO��4NH3+5O2����.���¸�ѹ4NO+6H2O��3NO2+H2O=2HNO3+NO��8HNO3+3Cu=3Cu��NO3��2+2NO+4H2O��
���������
�����Ѷȣ�һ��
3������� A��B��C��D��E�������ʶ���1��18��Ԫ���е�ijһԪ�أ����ǰ�ͼ��ʾ��ϵ�ת������֪AΪ���ʣ�
��1��д��A��E�Ļ�ѧʽ��A______��B______��C______��D______��E______��
��2��д��A��D��Ӧ�����ӷ���ʽ
A��D______��
��3��д��C��D��C��E��Ӧ�Ļ�ѧ����ʽ�����������ת�Ƶķ������Ŀ��
C��D______��
C��E______��
�ο��𰸣���1��A�ܺͿ����е������ڲ�ͬ�������·�����ͬ�ķ�Ӧ���������ܺ�ˮ��Ӧ��һ�ֵ��ʣ���1��18��Ԫ���еĵ����У�ֻ�н����Ʒ���Ҫ������A���ƣ�B�������ƣ�C�ǹ������ƣ�D���������ƣ�E��̼���ƣ��ʴ�Ϊ��Na��Na2O��Na2O2��NaOH��Na2CO3��
��2���ƺ�ˮ��Ӧ�����������ƺ�������ԭ����2Na+2H2O�T2NaOH+H2�����ʴ�Ϊ��2Na+2H2O�T2NaOH+H2����
��3�����������ܺͶ�����̼��Ӧ����̼���ƺ��������ܺ�ˮ��Ӧ�����������ƺ�������������������ԭ������ʽΪ��

��

��
�ʴ�Ϊ��

��

��
���������
�����Ѷȣ�һ��
4������� X��Y��ZΪ���ڱ���ǰ20������Ԫ�أ�ԭ������������X��Yԭ�ӵ�����������������Ӳ�����2����Z�����庬����ߵĽ���Ԫ�أ�
��1�����к��������ѧʽ��д����ȷ����______������ţ���
a��XO3-b��XO32-c��YO32-d��Y2O32-
��2��X��Y��ԭ�ӿɹ���ֻ�����Լ��ķǼ��Է��ӣ����ĵ���ʽ��______���ռ乹����______��
��3��Y����ۺ���������Ҫ�Ļ�����Ʒ��
����֪YO2������������ÿ����1mol��̬YO3���ų�98.3kJ�������÷�Ӧ���Ȼ�ѧ����ʽ��______��
��ʵ������ͬ������һ������Y���ʷֱ��ڿ������������г��ȼ�պ����ijɷ֣���������������
| ? | YO2 | YO3
����
94%��95%
5%��6%
����
97%��98%
2%��3%
|
Y�ڴ�����ȼ�ղ�����YO3�����ȿ������ٵ�ԭ����______��
����ȻZYO4�ȿ������Ʊ�Y���������ֿ�������ˮ�࣮ZYO4��X�����ڸ����·�Ӧ���õ����ֳ������壮ÿ����1molX���ʣ���4mol����ת�ƣ��÷�Ӧ�Ļ�ѧ����ʽ��______��
��4��Ϊ�˲ⶨijˮ����Ʒ�ɷ֣���ȡ10.0g��Ʒ�������е�ZԪ��ת��ΪZX2O4��������������ϡ�ᴦ����H2X2O4��Һ��ȡ����Һ�����1/100����KMnO4��Һ�ζ�����������ΪXO2����ԭ����ΪMn2+���������ȥ0.0200mol?L-1��KMnO4��Һ24.00mL������Ʒ��Z�������������������______��
�ο��𰸣�����������������Ӳ�����2����Ԫ����C��S����Ԫ�أ�����ԭ���������ε�����֪X��CԪ�أ�Y��SԪ�أ�Z�����庬����ߵĽ���Ԫ�أ�ӦΪCaԪ�أ�
��1��XO3-��X�Ļ��ϼ�Ϊ+5�ۣ�CԪ�ص�ԭ�������ֻ��4�����ӣ��������γ�+5�ۻ��������ѡ��ֱ�Ϊ��CO32-��SO32-��S2O32-������C��S�����Ĵ�����ʽ���ʴ�Ϊ��a��
��2��X��Y��ԭ�ӿɹ���ֻ�����Լ��ķǼ��Է��ӣ��÷���ΪCS2�������к���2���ļ���û�йµ��Ӷԣ�Ϊֱ���ͷ��ӣ�����ʽΪ
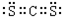
��
�ʴ�Ϊ��
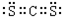
��ֱ���ͣ�
��3���ٸ�����д�Ȼ�ѧ����ʽ�ķ�����д��SO2������������ÿ����1mol��̬SO3���ų�98.3kJ��������Ӧ���Ȼ�ѧ����ʽΪSO2��g��+1/2O2��g���TSO3��g����H=-98.3KJ/mol��
�ʴ�Ϊ��SO2��g��+1/2O2��g���TSO3��g����H=-98.3KJ/mol��
������������Ӧ�Ƿ��ȿ��淴Ӧ���ڴ����и����ҷ��ȸ��࣬ʹƽ����������У����Դ����������������٣�
�ʴ�Ϊ��������O2Ũ�ȴ�λʱ���ڷ��ȶ࣬��ϵ�¶ȸߣ�ƽ����SO3�ֽ�ķ����ƶ���
��CaSO4��C�����ڸ����·�Ӧ���õ����ֳ������壬������ΪCO2��SO2��ÿ����1molC���ʣ���4mol����ת�ƣ���ÿ��1molC�μӷ�Ӧ��Ӧ��2mol����SO2��
��Ӧ�ķ���ʽΪ2CaSO4+C�T2CaO+CO2��+2SO2����
�ʴ�Ϊ��2CaSO4+C�T2CaO+CO2��+2SO2����
��4������������ԭ��Ӧ��ʧ�����غ��Ϲ�ϵʽ���㣬���������غ�ù�ϵʽCaC2O4��H2C2O4����������ԭ��Ӧ��ʧ������Ŀ��ȿ�֪5H2C2O4��2KMnO4������5CaC2O4��5H2C2O4��2KMnO4��
��5CaC2O4��5H2C2O4��2KMnO4
? 5mol? 5mol? 2mol
?n?n?0.0200mol?L-1��0.024L=4.8��10-4mol
n=5��4.8��10-4mol2=1.2��10-3mol
����10.0g��Ʒ��CaԪ�ص����ʵ���Ϊ100��1.2��10-3mol=0.12mol����Ʒ��CaO������Ϊ0.12mol��56g/mol=6.72g����������Ϊ6.7210��100%=67.2%��
�ʴ�Ϊ��67.2%��
���������
�����Ѷȣ���
5������� ��10�֣���֪A��B��C�ǵ��ʣ�����A�ǽ����������ʼ��ת����ϵ��ͼ��
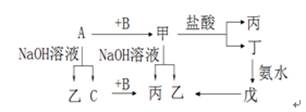
�ش��������⣺��1��д���������ʵĻ�ѧʽ����1�֣���
��1��A��________��B��________���ң�________��
����________������________���죺________
��2��д��A��NaOH��Һ�Ļ�ѧ����ʽ?��
д��������������ӷ���ʽ?��
�ο��𰸣���1���������֣�A��Al��B��O2���ң�Na AlO2������H2O������AlCl3���죺Al(OH)3
��2���������֣�2Al��2NaOH��2H2O��2Na AlO2��3H2?
Al3++3NH3��H2O=Al(OH)3��+3NH4+
������������������仯�����ת��
��������A����NaOH��Һ��Ӧ�����ж�Ϊ��������CΪ��������ΪNa AlO2��
���뵥��B�������ɼף����������ᷴӦ��Ҳ����NaOH��Һ��Ӧ��Ӧ������������Al2O3�����ʣ���BΪ��������Ϊˮ����ΪAlCl3��AlCl3�백ˮ�����죺Al(OH)3
�����Ѷȣ���