1、实验题 甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。
(1)甲组:沉淀分析法把一定量的混合物溶解后加入过量CaCl2,然后将所得沉淀过滤、洗涤、烘干、称量。确定CaCl2溶液是否过量的方法是_______________,洗涤沉淀并判断沉淀是否洗净的操作是_____________________。
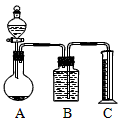
(2)乙组:气体分析法把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是_________________,选用该溶液后实验结果还是不准确,原因是_____________。
(3)请你设计一个与甲、乙两组操作不同的实验方案,测定混合物中Na2CO3的含量。方法:_________。用到的主要试剂:_______(至少2种)。用到的玻璃仪器:____________(至少2件)
参考答案:(1)静置,向上层清液中继续滴加CaCl2溶液,若无沉淀说明CaCl2已过量 ;沿玻棒向过滤器中的沉淀上加蒸馏水至淹没沉淀,静置使其全部滤出,重复2~3次,然后向滤液(洗涤液)中滴加AgNO3溶液判断是否洗净。
(2)饱和NaHCO3溶液 ;从A出来的气体中混有HCl,会与NaHCO3反应生成CO2
(3)滴定分析法(或中和滴定法、滴定法、用标准盐酸滴定一定量的混合物等) ;标准盐酸溶液、指示剂(甲基橙、酚酞) ;酸式滴定管、锥形瓶、 烧杯
本题解析:
本题难度:一般
2、实验题 粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验: ?
①取适量A进行铝热反应,产物中有单质B生成; ?
②另取20g?A全部溶于0.15L?6.0mol/L盐酸中,得溶液C; ?
③将①中得到的单质B和溶液C反应,放出1.12L(标准状况)气体,同时生成的溶液D中还残留有固体物质B; ?
④用KSCN溶液检验时,溶液D不变色。 ?
请填空:?
(1)①中引发铝热反应的实验操作是____,产物中的单质B是____。?
(2)②中所发生的各反应的化学方程式是____。?
(3)③中所发生的各反应的离子方程式是____。?
(4)若溶液D的体积仍视为0.15L,则该溶液中c(Mg2+)为____,c(Fe2+)为____。
参考答案:(1)“略”?
(2)Fe2O3?+?6HCl=2FeCl3?+?3H2O、MgO?+2HCl=MgCl2?+?H2O?
(3)Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+?
(4)0.67?mol/L;2.3?mol/L
本题解析:
本题难度:一般
3、实验题 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
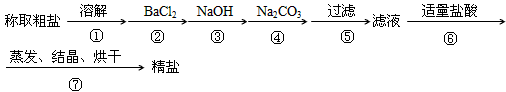
(1)判断BaCl2已过量的方法是___________________。
(2)第④步中,写出相应的离子方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
____________________。
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是____________________。
(4)为检验精盐纯度,需配制250mL 0.2mol/L NaCl(精盐)溶液,题图是该同学转移溶液的示意图,图中的错误是___________________________。
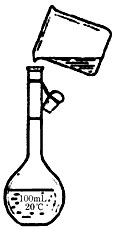
参考答案:(1)取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量(答案合理即可)
(2)Ca2++CO32-=CaCO3↓;Ba2++CO32-=BaCO3↓
(3)在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
(4)未用玻璃棒引流,未采用250mL容量瓶
本题解析:
本题难度:一般
4、选择题 下列制备气体的方法中合理的是( )
A.向饱和氯化钠溶液中滴加稀硫酸制备HCl
B.铜片与浓硫酸混合制备SO2
C.亚硫酸钠与w(H2SO4)=80%的硫酸反应制备SO2
D.大理石与浓硫酸反应制备SO2
参考答案:C
本题解析:
本题难度:一般
5、填空题 在实验室制取蒸馏水的装置中,温度计的水银球应位于______;烧瓶中应放几粒沸石(或碎瓷片),其作用是______;冷凝管中冷凝水的流向应当是______(流向用上口、下口、谁为进水口,谁为出水口表示).
参考答案:实验室制取蒸馏水的装置中,温度计的作用是测量蒸汽的温度,应位于蒸馏烧瓶支管口下沿;为防止液体暴沸,应加碎瓷片,冷凝管应从下口进水,上口出水,以保证水充满冷凝管,起到充分冷凝的作用,
故答案为:蒸馏烧瓶支管口下沿;防止暴沸;下口进水,上口出水.
本题解析:
本题难度:一般