1、选择题 制取普通玻璃的主要原料是
①Na2SiO3?②CaCO3?③CaSiO3?④SiO2?⑤Na2CO3?⑥CaO
A.①③④
B.②④⑥
C.②④⑤
D.③④⑤
参考答案:C
本题解析:略
本题难度:简单
2、选择题 2007年6月5日各大媒体报道了中国在南海北部成功钻获天然气水合物实物样品“可燃冰”,从而成为继美国、日本、印度之后第4个通过国家级研发计划采到水合物实物样品的国家。第28届国际地质大会提供的资料显示,海底有大量的天然气水合物,可满足人类1000年的能源需要。关于“可燃冰”的叙述不正确的是(C? )
A.“可燃冰”有可能成为人类未来的重要能源
B.“可燃冰”是一种比较洁净的能源
C.“可燃冰”提供了水可能变成油的例证
D.“可燃冰”的主要可燃成份是甲烷
参考答案:C
本题解析:可燃冰的主要成分是甲烷,不是由水生成的,所以选项C是错误的,水不可能生成汽油,其余都是正确的,答案选C。
本题难度:一般
3、选择题 下列不属于硅酸盐工业产品的是
[? ]
A.水泥
B.玻璃
C.陶瓷
D.化肥
参考答案:D
本题解析:
本题难度:简单
4、填空题 (共12分)钛是21世纪金属。下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
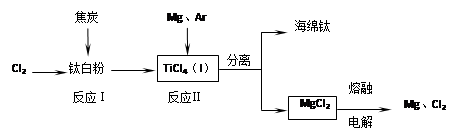
已知:① Mg(s)+Cl2 (g)=MgCl2 (s)? △H=-641 kJ・mol-1
② Cl2(g)+1/2Ti (s)=1/2TiCl4 (l)? △H=-385 kJ・mol-1
(1)钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的。
TiO2+发生水解的离子方程式为?。
(2)反应I在800~900℃下进行,还生成一种可燃性无色气体,该反应的化学方程式为?;
反应II的热化学方程式为?。
(3)该工艺流程中,可以循环使用的物质有?(填化学式)。
(4)在800℃~1000℃时电解TiO2也可制得海绵钛,装置如右图所示。图中b是电源的?极,阴极的电极反应式为?。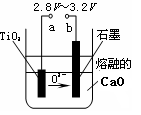
参考答案:(共12分)每空2分(1)TiO2++2H2O=H2TiO3↓+2H+(2分)
(2)TiO2+2Cl2+2C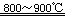
2Mg(s)+TiCl4(l)=2MgCl2(s)+Ti(s)? △H=-512 kJ・mol-1(2分,状态不写0分)
(3)Mg、Cl2(每空1分,共2分)
(4)正(2分)? TiO2+4e-=Ti+2O2-(2分)
本题解析:(1)TiO2+发生水解生成钛酸(H2TiO3)沉淀,说明水解程度很大,所以TiO2+发生水解的离子方程式为TiO2++2H2O=H2TiO3↓+2H+。
(2)根据元素的组成可知,可燃性无色气体应该是CO,所以该反应的化学方程式是TiO2+2Cl2+2C?TiCl4+2CO。根据盖斯定律可知,(①-②)×2即得到2Mg(s)+TiCl4(l)=2MgCl2(s)+Ti(s),所以该反应的反应热△H=(-641kJ/mol+385 kJ/mol)×2=-512 kJ/mol。
(3)根据转 化图可知,最后氯化镁电解又生成镁和氯气,二者可以循环使用。
(4)根据装置图可知,氧离子向b电极移动,所以与b相连的电极是阳极,因此b是电源的正极。电解池中阴极是得到电子的,所以阴极电极反应式是TiO2+4e-=Ti+2O2-。
点评:本题难度不是很大,考查的知识点较多、综合性较强,考查同学们新信息获取、处理及灵活运用所学知识(化学方程式、电极反应式的书写、盖斯定律以及电源正负极的判断等)进行分析问题、解决问题的能力。重点考查学生对化学知识的熟练掌握程度,以及灵活运用知识解决实际问题的能力。
本题难度:一般
5、填空题 钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉冶炼,常用赤铁矿、焦炭、空气和熔剂(石灰石)作原料。已知赤铁矿被还原剂还原时是逐级进行的,还原时温度及CO、CO2平衡混合气体中CO的体积分数的关系如下图:
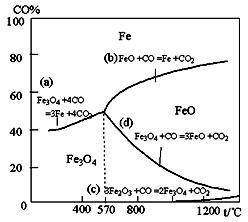
(1)铁在元素周期表中位于??周期???族
(2)在温度低于570℃时,还原分两阶段完成,在温度高于570℃时,依次发生的还原反应有:???(选用右图中的a、b、c、d填空)
(3)为减少高炉冶铁时,含CO的尾气排放,下列研究方向不可取的是???。
(a)其它条件不变,增加高炉的高度
(b)调节还原时的炉温
(c)增加原料中焦炭与赤铁矿的比例
(d)将生成的铁水及时移出
(4)已知下列反应数值:
反应序号
| 化学反应
| 反应热
|
①
| Fe2O3(s)+3CO(g)=2Fe(s)+3CO 2(g)
| △H1= -26.7kJ・mol-1
|
②
| 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)
| △H2= -50.8kJ・mol-1
|
③
| Fe3O4(s)+CO(g)=3FeO(s)+CO2 (g)
| △H3= -36.5kJ・mol-1
|
④
| FeO(s)+CO(g)=Fe(s)+CO2(g)?
| △H4
|
反应④△H4=?kJ・mol-1。
(5)1100℃时, FeO(s)+CO(g) 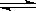 Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2gFeO,同时通入4.48LCO(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为:?。
Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2gFeO,同时通入4.48LCO(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为:?。
参考答案:

本题解析:略
本题难度:一般