| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《化学平衡》答题技巧(2017年最新版)(四)
参考答案:D 本题解析:A.16O和18O的物理性质不同,化学性质相似,A错误;B.同位素之间的转化不是化学变化,B错误;C.向2SO2(g)+O2(g) 本题难度:一般 4、选择题 乙酸、乙醇生成乙酸乙酯的反应是可逆反应,反应一段时间后,达到化学平衡状态。下列描述能说明乙酸与乙醇的酯化反应已经达到化学平衡状态的是(?) 参考答案:A 本题解析:在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态。平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,因此选项B不正确。选项A中反应速率的方向相反,且满足反应速率之比是相应的化学计量数之比,所以A正确。C中反应速率的方向是相同的,不正确。酯化反应中羧酸提供羟基,醇提供氢原子,选项D不正确,答案选A。 本题难度:简单 5、选择题 下列说法不正确的是(?) |


参考答案:A
本题解析:若加入少量醋酸钠固体,则CH3COOH CH3COO-+H+向左移动,α减小,但是Ka变大,A错误。常温下,反应
CH3COO-+H+向左移动,α减小,但是Ka变大,A错误。常温下,反应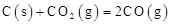 不能自发进行,△G=△H-T△S,△S>0△G>0,则该反应
不能自发进行,△G=△H-T△S,△S>0△G>0,则该反应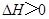 ,B正确。一定温度下,氯化铵水解离子方程式:NH+4+H2O
,B正确。一定温度下,氯化铵水解离子方程式:NH+4+H2O NH3・H2O+H+,若用KW表示的离子积,Kb表示氨水电离常数,则氯化铵水解平衡常数K=KW/Kb,C正确。由△H=E生-E反=+630KJ/mol,D正确。
NH3・H2O+H+,若用KW表示的离子积,Kb表示氨水电离常数,则氯化铵水解平衡常数K=KW/Kb,C正确。由△H=E生-E反=+630KJ/mol,D正确。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《常见的化学.. | |