| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《离子共存》高频试题预测(2017年最新版)(八)
参考答案:D 本题解析:NO3-、H+、SO32-发生氧化还原反应,NO3-、SO32-都减少;加入盐酸,Cl-增加,故D正确。 本题难度:一般 3、选择题 某无色溶液能与铝反应放出氢气,则该溶液中肯定不能大量共存的离子组是 ( ) |
参考答案:B
本题解析:某溶液与Al反应产生氢气,则该溶液为酸性或碱性溶液,且不是硝酸。A、该组离子在碱性条件下不能大量共存,在酸性条件下可以大量共存,错误;B、该组离子中的碳酸氢根离子在酸性或碱性的条件下都不能大量共存,正确;C、该组离子在酸性条件下不能大量共存,亚硫酸根离子、偏铝酸根离子与氢离子反应,在碱性条件下可以大量共存,错误;D、该组离子中的镁离子在碱性条件下与氢氧根离子反应生成氢氧化镁,不能大量共存,在酸性条件下可以大量共存,错误,答案选B。
考点:考查给定条件的离子大量共存的判断
本题难度:一般
4、填空题 某无色稀溶液X中,可能含有下表所列离子中的某几种。
| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
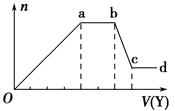
参考答案:(1)SiO32-、AlO2- CO32- Al(OH)3+3H+=Al3++3H2O
(2)Al3+、Mg2+、NH4+、Cl- NH4++OH-=NH3・H2O
本题解析:(1)因溶液是无色的,所以肯定不含Fe3+,加入盐酸后能形成的沉淀有Al(OH)3、H2SiO3,前者能溶于过量盐酸而后者不能,由图像知溶液中肯定含有AlO2-、SiO32-,Oa段发生反应的离子为AlO2-、SiO32-,ab段发生反应的离子为CO32-,bc段则是Al(OH)3溶解。(2)当向溶液中加入NaOH溶液时,生成的沉淀为Mg(OH)2、Al(OH)3,ab段是NH4+与OH-发生反应,因Mg2+、Al3+不能与CO32-、SiO32-、AlO2-共存,故此时溶液中的阴离子只有Cl-。
本题难度:一般
5、选择题 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1mol・L-1H2SO4溶液:K+、Ba2+、NO3-、Cl-
B.0.1mol・L-1NaOH溶液:Na+、Ca2+、I-、NH4+
C.0.1mol・L-1AlCl3溶液:K+、HCO3-、SO42-、NO3-
D.c(OH-)/c(H+)=l×l014的溶液:Ba2+、Na+、Cl-、NO3-
参考答案:D
本题解析:A.0.1mol・L-1H2SO4溶液:Ba2+不能大量共存;
B.0.1mol・L-1NaOH溶液:NH4+不能大量共存;
C.0.1mol・L-1AlCl3溶液:HCO3-不能大量共存。
故选D。
点评:审题时应注意题中给出的附加条件。
①酸性溶液(H+)、碱性溶液(OH-)、能在加入铝粉后放出可燃气体的溶液、由水电离出的H+或OH-=1×10-10mol/L的溶液等。
②有色离子MnO4-,Fe3+,Fe2+,Cu2+,Fe(SCN)2+。
③MnO4-,NO3-等在酸性条件下具有强氧化性。④S2O32-在酸性条件下发生氧化还原反应:S2O32-+2H+=S↓+SO2↑+H2O⑤注意题目要求“大量共存”还是“不能大量共存”。
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《酯》试题特.. | |