1、填空题 现有下列电解质溶液:① Na2CO3 ② NaHCO3 ③? ④CH3COONH4 ⑤NH4HCO3
④CH3COONH4 ⑤NH4HCO3
已知酸性H2CO3 >?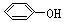 > HCO3-
> HCO3-
(1)常温下,物质的量浓度相同的① 、②、③溶液pH大小顺序为(填写序号):_____>_____>_____。
(2)写出⑤与足量NaOH溶液混合加热反应的离子方程式____________________。
(3)已知常温下CH3COONH4溶液呈中性,根据这一事实推测⑤溶液的pH_____7(填>、=或<)
(4)在温度t ℃时,pH=3的某水溶液中c(OH-)=10-9 mol/L在此温度下pH均为4的盐酸和(NH4)2SO4溶液中由水电离出的c(H+)之比为_________。
(5)将标准状况下的4.48 L氨气完全溶解在含0.1 mol HCl的水溶液中形成1 L溶液,所得溶液pH=9,其中离子浓度由大到小的顺序是_______________。
(6)常温下,pH=10的强碱AOH和pH=4的酸HnB等体积混合后溶液显酸性, AOH与HnB完全中和所得溶液呈_________性,其原因用离子方程式表示为__________________________。
参考答案:(1)①>③>②
(2)NH4++HCO3-+2OH- NH3↑+CO32-+2H2O
NH3↑+CO32-+2H2O
(3)>
(4)1:104
(5)c(NH4+)>c(Cl-)>c(OH-)>c(H+)?
(6)碱;Bn-+H2O HBn-1+OH-
HBn-1+OH-
本题解析:
本题难度:一般
2、选择题 盐酸、醋酸和碳酸氢钠是生活中常见的物质.下列表述正确的是( )
A.向NaHCO3溶液中加入与其等物质的量的NaOH固体,溶液的导电性增强
B.NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)
C.10 mL 0.10 mol?L-CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na)+>c(CH3COO-)>c(H+)>c(OH-)
D.完全中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同
参考答案:A
本题解析:
本题难度:一般
3、选择题 下列叙述中,能说明某化合物一定是弱电解质的是
A.该化合物的水溶液不导电
B.该化合物的饱和溶液导电能力较弱
C.该化合物在熔融时不导电
D.溶液中存在离子和溶质分子
参考答案:D
本题解析:弱电解质的水溶液也能导电,A选项错误.有的化合物在水中溶解度很小,所以离子浓度很小,导电能力很差,却是强电解质,如硫酸钡,B选项错误.熔融时不导电的化合物有可能是强电解质,如液态HCl等,C选项错误.只有D选项能说明该化合物只是部分发生了电离,表明该化合物是弱电解质.
本题难度:简单
4、选择题 下列物质属于电解质,而且可以导电的是( )
A.KCl固体
B.盐酸
C.乙醇
D.熔融的氧化铝
参考答案:A.KCl在水溶液中或熔融状态下能导电,是电解质;固体中有钾离子和氯离子,因没有自由移动的离子,不能导电,故A错误;
B.盐酸是氯化氢的水溶液,是混合物,不是化合物,所以不是电解质,故B错误;
C.乙醇是化合物,但其水溶液只存在乙醇分子,不导电,属于非电解质,故C错误;
D.熔融的氧化铝,是化合物,属于电解质,电离出自由移动的铝离子和氧离子,能导电,故D正确;
故选D.
本题解析:
本题难度:简单
5、选择题 下列物质中不属于电解质的是
[? ]
A.?NaOH?
B.?H2SO4?
C.?蔗糖?
D.?NaCl
参考答案:C
本题解析:
本题难度:简单