1��ѡ���� ������ʵ����֤����������������ʵ���? (? )
A��NaNO2��ˮ��Һ����ȫ����
B��HNO2��ʹʯ����Һ���
C�������ʵ���Ũ�ȵ�HNO2�ĵ���������������
D��0.1mol/L��HNO2��Һ��PHΪ2
�ο��𰸣�AB
���������ֻҪ˵���������Dz��ֵ���ļ��ɡ�A��ֻ��˵��NaNO2��ǿ����ʣ�B��ֻ��˵��HNO2���룬������˵��HNO2�Dz��ֵ��룻��C��˵��HNO2����������Ũ���٣�˵��HNO2�Dz��ֵ��룻D��0.1mol/L��HNO2��Һ��[H+]Ϊ0.01mol/L��˵��HNO2�Dz��ֵ��롣
�����Ѷȣ���
2��ѡ���� ��H2S�ı�����Һ�д�������ƽ��? ��H2S H++HS����HS��
H++HS����HS�� H++S2������֪K1��K2����ȡ�������ִ�ʩ�ȿ�����c(S2��)�������pH����ʹ����ƽ�������ƶ����ǣ�?��
H++S2������֪K1��K2����ȡ�������ִ�ʩ�ȿ�����c(S2��)�������pH����ʹ����ƽ�������ƶ����ǣ�?��
A����NaOH
B��ͨ��H2S����
C������
D������Na2S����
�ο��𰸣�D
�������������������ʵĵ���ƽ����ƶ��������ᡢ��Ρ�Ũ�ȼ��¶ȵ�Ӱ�졣
A.��NaOHʱ��OH��������Һ�е�H+��ƽ�����ƣ��ų�
B.ԭ��Һ�Ѿ����ͣ�ͨ��H2S���壬��ԭƽ�⼰��Ũ��û��Ӱ�죬�ų�
C.����ƽ�������ȷ�Ӧ������ʱƽ�����ƣ���Һ�е�c(S2��)��С���ų�
D.����Na2S���壬c(S2��)����ƽ�����ƣ�c(H+)��С��pH���ߣ���������
�ʴ�ΪD
�����Ѷȣ���
3������� ��ͬ�¶��µ�0.1Ħ/����0.01Ħ/��CH3COOH��Һ�У�CH3COOH�ĵ���ȣ�������
A������
B����
C������
D�����ܿ϶�
�ο��𰸣���ͬ�¶��µ�0.1Ħ/����0.01Ħ/��CH3COOH��Һ��
0.1mol/L��0.01mol/L��
��Ũ��ԽС������̶�Խ��
��0.01Ħ/��CH3COOH��Һ��CH3COOH�ĵ���ȴ�
��ѡB��
���������
�����Ѷȣ�һ��
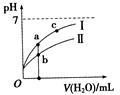
4��ѡ���� ��֪�±�Ϊ250CʱijЩ����ĵ���ƽ�ⳣ������ͼ��ʾ����ʱ��ϡ��CH3COOH��HClO�������ϡ��Һʱ����ҺpH���ˮ���ı仯������������Ϣ������˵����ȷ����
CH3COOH
| HClO
| H2CO3
|
Ka=1.8��10-5
| Ka=3��0��10-8
| Ka1=4��4��10-7?Ka2=4��7��10-11
|
?
A����ͬŨ�ȵ�CH3COONa��NaClO�Ļ����Һ�У�������Ũ�ȵĴ�С��ϵ�ǣ�
C(Na+)>C(ClO��)>C(CH3COO��)>C(OH��)>C(H+)
B����NaClO��Һ��ͨ������������̼�����ӷ���ʽΪ��2ClO��+CO2+H2O�T2HClO+CO32��
C��a��b��c������ʾ��Һ��ˮ�ĵ���̶�c>a>b
D��ͼ���У����ʾCH3COOH�����ʾHClO,����Һ������:c>b>a
�ο��𰸣�C
���������A�����������ǿ�ڴ����ᣬ������ͬŨ�ȵ�CH3COONa��NaClO�Ļ����Һ�У�ˮ��̶�CH3COO-< ClO������Һ������Ũ�ȵĴ�С��ϵ��C(Na+)>C(CH3COO��) >C(ClO��) >C(OH��)>C(H+)������B������������ƽ�ⳣ����֪����H2CO3> HClO> HCO3-,������NaClO��Һ��ͨ������������̼�����ӷ���ʽΪ��ClO��+CO2+H2O=HClO+HCO3��������C��a��b��c������ʾ��Һ��������Ũ�ȵĴ�С��ϵ��b>a>c��������Ũ��Խ��ʹˮ�ĵ���ƽ�������ƶ���ˮ�ĵ���̶�ԽС������ˮ�ĵ���̶�c>a>b����ȷ��D����������Աȴ�����ǿ�����Լ�����ͬ�����ˮʱ�����pHС�ڴ����ᣬ���Ԣ��ʾHClO�����ʾCH3COOH,��Һ�ĵ���������Һ�е�����Ũ���йأ�����Ũ��Խ������Խǿ��������Һ������: b>a>c������ѡC��
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ����
A��pH��5�����ᣬ�ټ�ˮ��ϡ1000������Һ��pH��8
B����ϡ������Һ���ȣ���ҺpHֵ����
C��pH=1��������c(H+)��pH=3�������100��
D����H2CO3��Һ�У�C(H+) ��C(CO32��-)��2��1
�ο��𰸣�C
�����������
�����Ѷȣ���