1、选择题 下列反应中,生成物的总能量小于反应物总能量的是
A.碳酸钙分解
B.酸碱中和
C.焦碳在高温下与水蒸气反应
D.Ba(OH)2.8H2O与NH4Cl(固体)的反应
参考答案:B
本题解析:生成物的总能量小于反应物总能量,说明该反应是放热反应,B正确,其余选项都是吸热反应,答案选B。
点评:该题是高考中的常见考点,属于基础性试题的考查。试题侧重对基础性知识的巩固与训练,有利于培养学生的应试能力,提高学生的学习效率。该题需要记住常见的放热反应和吸热反应,即一般金属和水或酸反应,酸碱中和反应,一切燃烧,大多数化合反应和置换反应,缓慢氧化反应如生锈等是放热反应。大多数分解反应,铵盐和碱反应,碳、氢气或CO作还原剂的反应等是吸热反应。
本题难度:简单
2、选择题 中和热测定实验中,下列操作一定会降低实验准确性的是( )
A.用滴定管取所用药品
B.NaOH溶液在倒入小烧杯时,有少量溅出
C.大、小烧杯体积相差较大,夹层间放的碎泡沫塑料较多
D.测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度
参考答案:B
本题解析:NaOH溶液在倒入小烧杯时,有少量溅出,实验中生成水的量减少,放出的热量减小,测得中和热的数值不准。
本题难度:一般
3、选择题 下列各表述与示意图一致的是


A.图①表示25℃时,用0.1 mol・L-1盐酸滴定20 mL 0.1 mol・L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2(g) + O2(g) 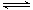 2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol・L-1 KMnO4酸性溶液与过量的0.1 mol・L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g) + H2(g)→CH3CH3(g);ΔH<0使用和未使用催化剂时,反应过程中的能量变化
参考答案:B
本题解析:根据图象中纵横坐标的含义,利用点、线来分析一个量发生变化随另外一个量如何变化,若变化趋势与图象中变化趋势一致,即为正确答案。A、0.1mol?L-1NaOH溶液的pH为13,用0.1mol?L-1盐酸滴定恰好中和时pH为7,由于浓度相同,则体积相同。但酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,故A错误;B、由于反应为放热反应,则升高温度,平衡逆向移动。所以平衡后升高温度K逆减小,而K正增大,且正逆反应的平衡常数互为倒数关系,故B正确;C、由于反应中生成的Mn2+对该反应能起催化剂的作用,从而使反应速率加快,因此与图像不符,C不正确;D、由于该反应是放热反应,所以反应物的总能量高于生成物的总能量,但图象描述的反应物的总能量低于生成物的总能量,因此D错误,答案选B。
本题难度:一般
4、选择题 白磷与氧可发生如下反应:P4 + 5O2 = P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P:a kJ・mol-1、P-O:b kJ・mol-1、P=O:c kJ・mol-1、O=O:d kJ・mol-1。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
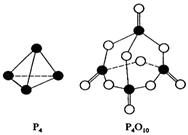
A.(6a+5d-4c-12b)kJ・mol-1
B.(4c+12b-6a-5d)kJ・mol-1
C.(4c+12b-4a-5d)kJ・mol-1
D.(4a+5d-4c-12b)kJ・mol-1
参考答案:A
本题解析:各化学键键能为P-P a kJ?mol-1、P-O b kJ?mol-1、P="O" c kJ?mol-1、O="O" d kJ?mol-1.
反应热△H=反应物总键能-生成物总键能,
所以反应P4+5O2=P4O10的反应热△H=6akJ?mol-1+5dkJ?mol-1-(4ckJ?mol-1+12bkJ?mol-1)=(6a+5d-4c-12b)kJ?mol-1,
故选:A。
点评:考查反应热与化学键键能的关系,难度中等,注意从物质能量、键能理解反应热。
本题难度:简单
5、选择题 下列离子方程式正确的是(? )
A.碳酸氢铵溶液与足量氢氧化钠溶液反应: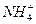 +OH-====NH3・H2O
+OH-====NH3・H2O
B.Fe(OH)3与氢碘酸溶液混合:Fe(OH)3+3H+====Fe3++3H2O
C.电解精炼铜的阴极反应是:Cu2++2e-====Cu
D.1 mol・L-1的NaAlO2溶液和2.5 mol・L-1的HCl等体积互相均匀混合:2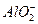 +5H+====Al(OH)3↓+Al3++H2O
+5H+====Al(OH)3↓+Al3++H2O
参考答案:CD
本题解析:A项中,NaOH足量,应放出NH3,A项错。B项中,Fe3+与I-不能共存。C项正确。D项由于HCl过量,故产物有Al(OH)3,也有Al3+,正确。
本题难度:简单