|
|
|
高考化学知识点归纳《盐类水解的原理》试题预测(2017年最新版)(四)
2017-11-11 02:33:41
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、填空题 某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol・L-1的MgCl2溶液中各加入10滴2 mol・L-1 NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
实验序号
| 加入试剂
| 实验现象
| Ⅰ
| 4 mL 2 mol・L-1 HCl 溶液
| 沉淀溶解
| Ⅱ
| 4 mL 2 mol・L-1 NH4Cl 溶液
| 沉淀溶解
|
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程 。
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因 。
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是 。
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是 。
(5)乙同学继续进行实验:向4 mL 2 mol・L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是 。
③乙同学这样配制混合溶液的理由是 。
参考答案:(1)Mg(OH)2(s)  Mg2+(aq)+2OH -(aq)(1分),盐酸中的H+与OH-中和使得OH-浓度减小平衡右移(1分),沉淀溶解 Mg2+(aq)+2OH -(aq)(1分),盐酸中的H+与OH-中和使得OH-浓度减小平衡右移(1分),沉淀溶解
(2)NH4++H2O  NH3・H2O+H+(2分) NH3・H2O+H+(2分)
(3)排除实验Ⅰ、Ⅱ中(1分)溶剂水使沉淀溶解的可能性(1分)(只答“4 mL水不能使沉淀溶解”给1分)
(4)溶液中c(NH4+)较大,NH4+结合OH-使沉淀溶解(2分)
(5)①沉淀溶解(1分) ②混合溶液显碱性,c(H+)非常小(1分,或答“H+不与OH-结合”), c(NH4+)较大(1分,或答“c(NH4+)与NH4Cl溶液接近”)能确定是NH4+结合OH-使沉淀溶解
本题解析:(1)Mg(OH)2存在沉淀溶解平衡:Mg(OH)2(s)  Mg2+(aq)+2OH -(aq),加入HCl后,H+与OH?反应,使OH?浓度减小,沉淀溶解平衡向右移动,Mg(OH)2沉淀溶解。 Mg2+(aq)+2OH -(aq),加入HCl后,H+与OH?反应,使OH?浓度减小,沉淀溶解平衡向右移动,Mg(OH)2沉淀溶解。
(2)NH4Cl为强酸弱碱盐,NH4+发生水解反应,离子方程式为:NH4++H2O  NH3・H2O+H+ NH3・H2O+H+
(3)实验Ⅰ、Ⅱ加入溶液,水增多,所以该实验的目的是:排除实验Ⅰ、Ⅱ中溶剂水使沉淀溶解的可能性。
(4)NH4+能与OH?结合,生成弱电解质NH3?H2O,所以溶液中c(NH4+)较大,NH4+结合OH-使沉淀溶解。
(5)①所加的混合液pH约为8,为碱性,所以沉淀溶解,可证明第二种猜测成立。
②混合液pH约为8,显碱性,c(H+)非常小,而NH4+少量溶解,c(NH4+)浓度较大,可确定沉淀溶解的原因是NH4+与OH?反应,促进沉淀溶解平衡向右移动。
考点:本题考查沉淀溶解平衡、盐类的水解、实验方案的分析。
本题难度:困难
2、选择题 下列有关说法正确的是
A.反应NH3(g)+HCl(g)= NH4Cl(s)在室温下可自发进行,则该反应的△H<0
B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.CH3COOH溶液加水稀释后,电离平衡正向移动,溶液中的c(CH3COO-)增大
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
|
参考答案:A
本题解析:A项根据ΔG=ΔH-TΔS,该反应正反应ΔS<0,而ΔG<0,所以ΔH<0,A项正确。B当镀层破损后,均形成原电池,锡和铁的原电池中铁做负极,腐蚀,而锌和铁的原电池中锌为负极,铁不腐蚀,故B错误;C项CH3COOH溶液加水稀释后,CH3COOH的电离平衡向电离的方向移动,则n(CH3COO-)增大,但是由于体积变大,c(CH3COO-)减小,故C错误。D项Na2CO3溶液中加入少量Ca(OH)2固体,化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,生成NaOH,溶液pH增大,同时会抑制溶液中的CO32--的水解,因此CO32-水解程度会减小,但溶液的pH会增大。
考点:反应自发性的判据;金属的腐蚀和防护;弱电解质的电离平衡和盐类的水解平衡
本题难度:一般
3、选择题 下列溶液中各微粒的浓度关系不正确的是
A.0.1mol・L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+)
B.0.1mol・L-1 NH4Cl溶液中:c(NH4+)+c(NH3?H2O)=c(Cl-)
C.0.1mol・L-1NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)=c(HCO3-)+c(CO32-)+c(OH-)
D.等体积、等物质的量浓度的CH3COONa和弱酸CH3COOH混合后的溶液中:c(CH3COO-)
|
参考答案:
本题解析:
本题难度:一般
4、选择题 100mL0.1mol/L的下列溶液中,阴离子总数多少的排列顺序正确的是
①CaCl2 ②CH3COONa ③NaCl ④Na2CO3
A.①>④>③>②
B.①>④>③=②
C.①>④=③=②
D.①>④>②>③
参考答案:A
本题解析:①氯化钙阴离子的物质的量为:0.1L×0.1mol/L×2=0.02mol。②醋酸钠中阴离子的物质的量为:0.1L×0.1mol/L=0.01mol,又因为醋酸根水解,故小于0.01mol。③氯化钠中阴离子物质的量为:0.1L×0.1mol/L=0.01mol。④碳酸钠中阴离子的物质的量为:0.1L×0.1mol/L=0.01mol,由于碳酸根水解,CO32-+H2O HCO3-+OH-故大于0.01mol。故①>④>③>②。
HCO3-+OH-故大于0.01mol。故①>④>③>②。
考点:盐类水解
本题难度:一般
5、选择题 下列关于电解质溶液的正确判断是
[? ]
A.在pH = 12的溶液中,K+、Cl-、HCO3-、Na+可以大量共存
B.在pH= 0的溶液中,Na+、NO32-、SO32-、K+可以大量共存
C.由0.1 mol一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH = B++OH-
D.由0.1 mol一元酸HA溶液的pH=3, 可推知NaA溶液存在A-+H2O 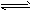 ?HA+OH-
?HA+OH-
参考答案:D
本题解析:
本题难度:一般
 HCO3-+OH-故大于0.01mol。故①>④>③>②。
HCO3-+OH-故大于0.01mol。故①>④>③>②。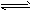 ?HA+OH-
?HA+OH-