1��ʵ���� ��1��ij��ȤС����ʵ����̽����ҵ�ϳ�����Ļ�ѧԭ����
�ٰ��Ĵ�������ͼa��̽�����Ĵ������ļ���װ�ã�ʵ���й۲쵽��ƿ�в�˿���ֺ��ȣ��к���ɫ�������ɻ���̲��������̵ijɷ��� ���ѧʽ����
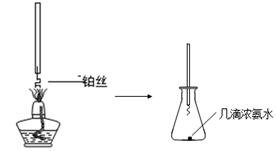

ͼa ͼb
��NO2�����գ���ͼb��ʾ����һƿNO2������ˮ���У���ˮ���ƿ�����Ƭ���ɹ۲쵽�������� ��
��2������������Һ��Fe3+ˮ������ػ�ɫ������Fe(NO3)3��ҺΪ�������ʵ��̽��Ӱ������ˮ��̶ȵ����ء�
��д��Fe(NO3)3ˮ������ӷ���ʽ ��
�ڲ���ʾ������±�ʵ�鷽������ơ�
��ѡ���ϣ�0.05mol?L-1Fe(NO3)3��0.5mol?L-1Fe(NO3)3��1.0mol?L-1HNO3��1.0mol?L-1NaOH��NaHCO3���塢����ˮ����ˮ����pH�Ƽ���������������
����Ӱ������
| ʵ�����
| Ԥ������ͽ���
|
��Һ�������
| ȡ����0.5mol?L-1Fe(NO3)3���Թ��У����뼸��1mol?L-1HNO3��
| �ػ�ɫ��Һ��ɫ��dz��˵����Һ������ǿ������Fe(NO3)3��ˮ�⡣
|
�ε�Ũ��
|
|
|
|
|
|
�ο��𰸣���1������4�֣��� NH4NO3 ��2�֣�
�� ����ƿ�к���ɫ����ʧ������ƿ�е�Һ�������� ��2�֣�
��2������12�֣�
�� Fe3+ + 3H2O  Fe(OH)3 + 3H+ ��2�֣�
Fe(OH)3 + 3H+ ��2�֣�
�ڣ�ע�������ı����Ҳ���֣�ÿ��2�֣���10�֣�
Ӱ������
ʵ�����
Ԥ������ͽ���
���ε�Ũ��
����Ͳȡ10mL Fe(NO3)3���ձ��У���pH�Ʋ��pHֵ����ȡ90mL����ˮ�����ձ�����ֽ��裬����pH�Ʋ��pHֵ��
ǰ����pHֵ֮��С��1��˵����ˮϡ�ͺ�ƽ�����ƣ����ɸ����H+��������Fe(NO3)3Ũ�ȣ�����Fe(NO3)3ˮ�⡣
����ε�Ũ��
��pH�Ʒֱ�ⶨ0.05mol?L-1Fe(NO3)3��0.5mol?L-1Fe(NO3)3��pH�����Ƚϴ�С��
������Һ��pHֵ֮��С��1��˵������c(Fe(NO3)3)������Fe(NO3)3ˮ�⡣
����ε�Ũ��
ȡ����0.5mol?L-1Fe(NO3)3���Թ��м�������NaHCO3���塣
��Һ��ɫ���˵����������NaHCO3����ɼ���c(H+)�ٽ�Fe(NO3)3ˮ�⡣
����ε�Ũ��
ȡ����0.5mol?L-1Fe(NO3)3���Թ��м��뼸��1.0mol?L-1NaOH
��������ɫ�������ػ�ɫ��Һ�����ɫ��˵������NaOH�ɼ���c(H+)�ܴٽ�Fe(NO3)3ˮ�⡣
�������¶�
ȡ����0.5mol?L-1Fe(NO3)3���Թ��У����þƾ��Ƽ���һ��ʱ�䣬�۲���Һ��ɫ
���Ⱥ���Һ��ɫ���˵�������¶ȴٽ�Fe(NO3)3ˮ�⡣
��۽����¶�
ȡ����0.5mol?L-1Fe(NO3)3���Թ��У��ٽ��Թ����ڷ��б�ˮ�������ձ���һ��ʱ�䣬�۲���Һ��ɫ
�ػ�ɫ��Һ��ɫ��dz��˵�������¶�������Fe(NO3)3ˮ�⡣
�����������1���ٰ�����������������������NO��ˮ��NO������е�������Ӧ���ɺ���ɫ�����������������������ˮ��Ӧ�����������ɣ������백����Ӧ���ɰ�ɫ��������泥�����̵ijɷ���NH4NO3��
�ڶ�����������ˮ�������������ɫ����NO��ͬʱƿ��ѹǿ��С�����Կ�������ƿ�ں���ɫ������ʧ������ƿ�е�Һ����������
��2����Fe(NO3)3ˮ�������������������ᣬ���ӷ���ʽΪFe3+ + 3H2O  Fe(OH)3 + 3H+
Fe(OH)3 + 3H+
��Ӱ����ˮ��̶ȵ�������Ũ�ȡ��¶ȡ�����������ˮ������ӷ���ʽ�ж�����������Ũ��ƽ�������ƶ����ɲ��ò�ͬŨ�ȵ�Fe(NO3)3��Һ������ʵ�飬�ⶨ��Һ��pH���ж�ˮ��̶ȵĴ�С������H+ Ũ��ƽ�������ƶ�����Һ�ػ�ɫ��dz��ˮ�ⷴӦ�ɿ������кͷ�Ӧ���淴Ӧ�����������ȷ�Ӧ�������¶�ƽ�⣬�����ƶ�����Һ�ػ�ɫ�������ʵ�����±���
Ӱ������
ʵ�����
Ԥ������ͽ���
���ε�Ũ��
����Ͳȡ10mL Fe(NO3)3���ձ��У���pH�Ʋ��pHֵ����ȡ90mL����ˮ�����ձ�����ֽ��裬����pH�Ʋ��pHֵ��
ǰ����pHֵ֮��С��1��˵����ˮϡ�ͺ�ƽ�����ƣ����ɸ����H+��������Fe(NO3)3Ũ�ȣ�����Fe(NO3)3ˮ�⡣
����ε�Ũ��
��pH�Ʒֱ�ⶨ0.05mol?L-1Fe(NO3)3��0.5mol?L-1Fe(NO3)3��pH�����Ƚϴ�С��
������Һ��pHֵ֮��С��1��˵������c(Fe(NO3)3)������Fe(NO3)3ˮ�⡣
����ε�Ũ��
ȡ����0.5mol?L-1Fe(NO3)3���Թ��м�������NaHCO3���塣
��Һ��ɫ���˵����������NaHCO3����ɼ���c(H+)�ٽ�Fe(NO3)3ˮ�⡣
����ε�Ũ��
ȡ����0.5mol?L-1Fe(NO3)3���Թ��м��뼸��1.0mol?L-1NaOH
��������ɫ�������ػ�ɫ��Һ�����ɫ��˵������NaOH�ɼ���c(H+)�ܴٽ�Fe(NO3)3ˮ�⡣
�������¶�
ȡ����0.5mol?L-1Fe(NO3)3���Թ��У����þƾ��Ƽ���һ��ʱ�䣬�۲���Һ��ɫ
���Ⱥ���Һ��ɫ���˵�������¶ȴٽ�Fe(NO3)3ˮ�⡣
��۽����¶�
ȡ����0.5mol?L-1Fe(NO3)3���Թ��У��ٽ��Թ����ڷ��б�ˮ�������ձ���һ��ʱ�䣬�۲���Һ��ɫ
�ػ�ɫ��Һ��ɫ��dz��˵�������¶�������Fe(NO3)3ˮ�⡣
���㣺���鰱���Ĵ��������������������գ������ӵ�ˮ�⼰Ӱ��ˮ��̶ȵ�������ʵ�����
�����Ѷȣ�����
2������� д����������Һ��ˮ�����ӷ���ʽ��
��1����e���Σϣ������� ��
��2����a�� ��
��3���ˣ��ãϣ� �� ��
�ο��𰸣���1��Fe3+ ��3H2O��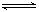 ��Fe(OH)3���� 3H +
��Fe(OH)3���� 3H +
��2��F-����H2O��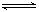 HF���� OH��
HF���� OH��
��3��CO32-��H2O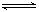 HCO3-�� OH�� ;
HCO3-�� OH�� ;
HCO3-��H2O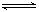 H2CO3�� OH��
H2CO3�� OH��
�����������1����Ԫ����������һ��ˮ��
��3����Ԫ������������Ҫ�ֶಽˮ��
�����Ѷȣ�һ��
3��ѡ���� ������������ʵ���Ũ�ȵ�NaCl��NaF��Һ�У����������������
A.ǰ�߶�
B.���߶�
C.һ����
D.���ж�
�ο��𰸣�B
�����������ȷ�𰸣�B
NaF��ǿ�������Σ�F����H2O HF��OH�D ,�ٽ�ˮ���롣�������ɵ�OH�D�࣬��������������Ⱥ��߶ࡣ
HF��OH�D ,�ٽ�ˮ���롣�������ɵ�OH�D�࣬��������������Ⱥ��߶ࡣ
�����Ѷȣ�����
4��ѡ���� ���ᱵ[(CH3COO)2Ba��H2O]��һ��ýȾ�����й�0.1 mol/L���ᱵ��Һ������Ũ�ȱȽϲ���ȷ����
A.c(Ba2+)��c(CH3COO-)��c(OH-)��c(H+)
B.c(H+)+2c(Ba2+)��c(CH3COO-)+c(OH-)
C.c(H+)��c(OH-)-c(CH3COOH)
D.2c(Ba2+)��c(CH3COO-)+c(CH3COOH)
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ���ǣ�
A�������´�����Ӳ����ܴ�����pH>7�ļ�����Һ��
B����0.1mol��LNa2SO3����Һ�м�������NaOH���壬c(Na+)����c(SO32