1��ѡ���� ����ͼ��ʾװ�ý���ʵ�飬������������ȷ���� ��?��

A��K��N����ʱ��������ʴ
B��K��N����ʱ��ʯī�缫��������
C��K��M����ʱ��һ��ʱ�����Һ��pH����
D��K��M����ʱ��ʯī�缫��Ӧʽ��4OH����4e��=2H2O��O2��
�ο��𰸣�D
���������K��N����ʱ������ԭ��أ��������ⸯʴ��A��B��ȷ��K��M����ʱ���缫��ӦʽΪ������2Cl����2e��=Cl2����������2H����2e��=H2����D�����
�����Ѷȣ�һ��
2��ѡ���� ����ͼ��ԭ��ز����ĵ�ѹ������ǿ�Ⱦ��������⡢���Ҫ��Ϊ���뻯���١���Ϊ��װ���еĵ缫��š�����˵���������
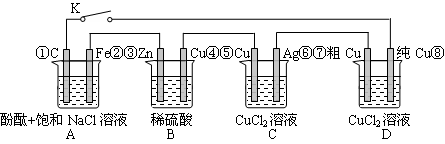
A����K�պ�ʱ��Aװ�÷���������ʴ���ڵ�·������Դ
B����K�Ͽ�ʱ��Bװ��пƬ�ܽ⣬����������
C����K�պϺ�������·�е��ӵ���������Ϊ�١��ࣻ�ߡ��ޣ��ݡ��ܣ��ۡ���
D����K�պϺ�A��Bװ����pH���C��Dװ����pH����
�ο��𰸣�A
�������������װ�ÿ��жϣ�Bװ����ԭ��أ�����п�Ǹ�����ͭ��������A��C��D�ǵ��ء�A����K�պ�ʱ��Aװ���е����븺��������������������������A����ȷ��B����K�Ͽ�ʱ��Bװ��пƬֱ����ϡ���ᷴӦ��п�ܽ⣬������������B��ȷ��C����K�պϺ�Bװ����ԭ��أ�����п�Ǹ�����ͭ��������������·�е��ӵ���������Ϊ�١��ࣻ�ߡ��ޣ��ݡ��ܣ��ۡ��ڣ�C��ȷ��D����K�պϺ�Aװ���ǵ��أ���Ӧ���������������ɣ�pH���Bװ����ԭ��أ������ӷŵ磬�����Һ��pH���Cװ���൱�ڵ�ƣ�Dװ���Ǵ�ͭ�ľ��������C��Dװ����pH���䣬D��ȷ����ѡA��
�����Ѷȣ�һ��
3��ѡ���� ���й��ڽ�����ʴ��˵���в���ȷ���ǣ�?��
A��������ʴ�ı����ǽ���ԭ��ʧȥ���Ӷ�������
B��������ʴһ�������ѧ��ʴ�͵绯ѧ��ʴ
C�����������Ի����лᷢ�����ⸯʴ
D�����Ľ���һ�����Է����绯ѧ��ʴ
�ο��𰸣�C
������������������Ի����лᷢ�����ⸯʴ��ѡ��C����ȷ������ѡ�����ȷ�ģ���ѡC��
�����������ǻ���������Ŀ��飬��Ҫ�ǿ���ѧ���Խ�����ʴ����Ϥ�˽�̶ȣ�ּ�ڹ��̣����ѧ����Ӧ���������ѶȲ���ס���ɡ�
�����Ѷȣ���
4������� ȫ����ÿ���������ʴ��ɵ�ֱ�Ӿ�����ʧԼ��7000����Ԫ���ҹ��������ʴ��ɵ���ʧռ����������ֵ��4%��
��1��������ݲ�ͬԭ���������ֹ������ʴ������������ʩ��
��______��
��______��
��2����д����ϡ�����ȥ����Ļ�ѧ��Ӧ����ʽ��______��
�ο��𰸣���1�����ڳ�ʪ�Ļ����������绯ѧ��ʴ��Ϊ��ֹ������ʴ����ֹ������ʴ�ؼ�����������ˮ���������Խ��б������������Ϳ�͡�ˢ�ᡢ����ƽ����ȣ��������Ըı�����ڲ��ṹ���Ƴɲ���֣��ȣ�
�ʴ�Ϊ���ı�����ڲ��ṹ���Ƴɲ���֣���ˢ�ᣨͿ�͡�����ƽ�������
��2���������Ҫ�ɷ��������������Ժ��ᷴӦ�����κ�ˮ����Fe2O3+3H2SO4�TFe2��SO4��3+3H2O��
�ʴ�Ϊ��Fe2O3+3H2SO4�TFe2��SO4��3+3H2O��
���������
�����Ѷȣ�һ��
5��ѡ���� ��ͼ��ģ��绯ѧ��Ӧ��װ��ͼ�������й������У��������
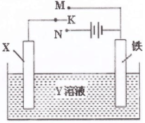
A��XΪ̼����YΪNaCl��Һ������K����N������Һ������������̼��
B��XΪп����YΪNaCl��Һ������K����N�����ɼ������ĸ�ʴ���÷���Ϊ��������������������
C��XΪͭ����YΪCuSO4��Һ������K����M����ͭ�����������ӣ����·�еĵ�������ͭ��
D��XΪͭ����YΪCuSO4��Һ������K����N�����������������ӣ���Һ��Cu2+Ũ�Ȳ���ı�
�ο��𰸣�AB
�����������������N��ʱ��X�����NaCl��Һ�������������������ڵ�·������������������������������A������ӵ�Դ�ĵ����У�п��������ʴ�������������ܱ������������������ӵ�Դ������������������������������������������B������K����M����ͭ����ԭ��ص����������������������·�е�������ͭ�����ڵ�·CuSO4��Һ�е�Cu2+�Ƶ������Ϸ�����ԭ��Ӧ����������ͭ������ͭ���ϣ�ͭ���������ӣ���C��ȷ����������N��ʱ��ͭ������������ӦΪCu��2e��==Cu2+������������CuSO4��Һ�е�Cu2+�Ƶ������Ϸ�����ԭ��Ӧ��Cu2++2e��==Cu���������������ӣ���������Cu2+����������������Cu2+�����������Һ��Cu2+��Ũ�ȱ��ֲ��䣬��D��ȷ��
�����Ѷȣ�һ��