1、选择题 含SO2的烟气会形成酸雨,工业上常利用Na2SO3溶液作为吸收液脱除烟气中的SO2。随着SO2的吸收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是:
A.Na2SO3溶液中存在:
B.已知NaHSO3溶液 ,该溶液中:
,该溶液中: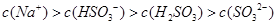
C.当吸收液呈中性时:
D.当吸收液呈酸性时:
参考答案:C
本题解析:亚硫酸钠溶于水SO32-水解,溶液显碱性,由于第二步的水解程度小于第一步的水解程度,所以应该是c(HSO3-)>c(H2SO3),A不正确;已知NaHSO3溶液pH<7,这说明HSO3-的电离程度大于HSO3-的水解程度,所以c(SO32-)>c(H2SO3),B不正确;根据电荷守恒可知c(Na+)+c(H+)=c(OH-)+2c(SO32-)+c(HSO3-),溶液显中性,则c(H+)=c(OH-),所以c(Na+)=2c(SO32-)+c(HSO3-),C正确;当溶液显酸性时,该溶液不一定恰好是亚硫酸氢钠,因此c(Na+)不一定等于c(SO32-)+c(HSO3-)+c(H2SO3),即选项D不正确,答案选C。
点评:该题是高考中的常见题型,属于综合性试题的考查,对学生的思维能力提出了较高的要求,本题贴近高考,综合性强,侧重对学生能力的培养,意在培养学生的逻辑推理能力和创新思维能力。该题的关键是在明确反应原理的基础上利用好几种守恒关系,即电荷守恒、物料守恒以及质子守恒,然后结合题意灵活运用即可。
本题难度:简单
2、选择题 下列各组离子,能在指定溶液中大量共存的是
[? ]
①无色溶液中:K+,Br-,Na+,HCO3-
②使pH试纸变深蓝的溶液中:K+,CO32-,Na+,AlO2-
③水电离产生的c(H+)=10-12mol・L-1的溶液中:ClO-,CO32-,NO3-,NH4+,SO32-
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,Na+,SO42-
⑤使甲基橙变红的溶液中:MnO4-,NO3-,Na+,SO42-,Fe3+
⑥PH=0溶液中:Fe2+,Al3+,NO3-,Cl-
A.①③⑥
B.①②④⑤
C.①④⑤
D.③⑥
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列各组的离子,能在溶液中大量共存的是(? )?
A.Na+ 、H+、SO42-、HCO3-
B.Cu2+、SO42-、Ba2+、Cl-
C.Na+、 K+、Cl-、 NO3-
D.Fe2+、NO3-、Cl-、H+、
参考答案:C
本题解析:A不能,氢离子与碳酸氢根离子不能共存.
B不能,钡离子与硫酸根离子不能共存.
C可以.
D不能,硝酸根离子在氢离子存在的情况下能表现出强氧化性,可以将+2价铁离子氧化成+3价.
本题难度:一般
4、选择题 某无色溶液中加入氢氧化铝,氢氧化铝迅速溶解,则该溶液中一定能够大量共存的离子组是
A.K+、Ba2+、NO3-、Cl-
B.Na+、K+、CO32―、SO42-
C.Na+、K+、Fe2+、NO3-
D.Na+、Fe3+、Cl―、SCN―
参考答案:A
本题解析:略
本题难度:简单
5、选择题 常温下,下列各组离子在指定溶液中能大量共存的是( )
A.加入铝粉产生H2的溶液中:Fe2+、Na+、SO42-、ClO-
B.滴入酚酞显红色的溶液中:NH4+、Mg2+、AlO2-、NO3-
C.pH=1的溶液中:Fe3+、Cl-、NO3-、K+
D.c(SO32-)=0.1mol?L-1的溶液中:Ca2+、MnO4-、SO42-、H+
参考答案:A、加入铝粉产生H2的溶液可能为酸或碱的溶液,若为碱,OH-、Fe2+结合生成沉淀,若为酸,H+、Fe2+、ClO-发生氧化还原反应,则一定不能大量共存,故A错误;
B、滴入酚酞显红色的溶液显碱性,OH-、NH4+结合生成弱电解质,OH-、Mg2+结合生成沉淀,NH4+与AlO2-还发生相互促进的水解,则一定不能大量共存,故B错误;
C、pH=1的溶液中有大量的H+,该条件下该组离子之间不反应,则能大量共存,故C正确;
D、因Ca2+、SO42-结合生成微溶物,SO32-、MnO4-、H+发生氧化还原反应,则一定不能大量共存,故D错误.
故选C.
本题解析:
本题难度:一般