1��ѡ���� ���й��ڳ����ܽ�ƽ���˵���������? (? )
A�����ܵ������ˮ�д��ڳ����ܽ�ƽ�⣬����һ�ֶ�̬ƽ��
B��Kspֻ�����ܵ���ʵ����ʺ��¶��йأ����������������Һ�����ӵ�Ũ����
C��Ksp��ӳ��������ˮ�е��ܽ���������ֱ�Ӹ���Ksp����ֵ��С�Ƚϵ������ˮ�е��ܽ�������С
D������ͨ��Ũ���̣�Qc����Ksp����Դ�С�����жϳ����ܽ�ƽ����ƶ�����
�ο��𰸣�C
���������������Ҫ�漰���ܶȻ����������⡣�������ܶȻ����������ʵ�һ�����ʣ���ֻ��������ʵı������ʺ��������¶��йأ������ܽ�ƽ�����ܽ���ᾧ�����̵Ķ�̬ƽ�⡣������ѧƽ��һ������Ũ�������ܶȻ��Ĵ�С�ж�ƽ���ƶ��ķ���ÿһ�����ʵ��ܶȻ������ĵ�λ�Լ������Dz�һ���ģ�����ֻͨ����ֵ��С���Ƚϵ������ˮ�е��ܽ���������A.B.D����ȷ�ġ�ӦѡC��
�����Ѷȣ�һ��
2������� (4��)����ͼ��ʾ��������Ϊ��Һ��pH��������ΪZn2����[Zn(OH)4]2�������ʵ���Ũ�ȵĶ�����
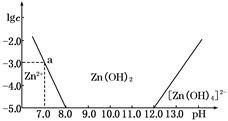
�ش��������⣺
(1)��ZnCl2��Һ�м�������������������Һ����Ӧ�����ӷ���ʽ�ɱ�ʾΪ_______________��
(2)��ͼ�����ݼ���ɵ�Zn(OH)2���ܶȻ�Ksp��____________________��
(3)ij��Һ�к�Zn2����Ϊ��ȡZn2�����Կ�����Һ��pH�ķ�Χ��__________________��
(4)25��ʱ��PbCl2Ũ��������Ũ�ȱ仯���±���
c(HCl)
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
(mol/L)
| 0.50
| 1.00
| 2.04
| 2.90
| 4.02
| 5.16
| 5.78
|
103c(PbCl2)
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
(mol/L)
| 5.10
| 4.91
| 5.21
| 5.90
| 7.48
| 10.81
| 14.01
|
�����ϱ������ж�����˵����ȷ����________��
A����������Ũ�ȵ�����PbCl2������ܽ���ȱ�С���ֱ��
B��PbCl2������0.50 mol/L�����е��ܽ��С���ڴ�ˮ�е��ܽ��
C��PbCl2����Ũ���ᷴӦ����һ���ѵ����������(�������)
D��PbCl2��������ڱ���ʳ��ˮ
�ο��𰸣�(4��) (1)���ӷ���ʽ�ɱ�ʾΪ__ Zn2����4OH��===[Zn(OH)4]2����
(2) Ksp��__10��17_��(3) pH�ķ�Χ��__8.0��pH��12.0��
(4)��ȷ����_ A��B��C��D��
�����������
�����Ѷȣ�һ��
3������� ��һ�̶��ݻ����ܱ������н��������·�Ӧ��
CO2(g) + H2(g)?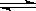 ?CO(g) + H2O(g)����ƽ�ⳣ���˺��¶�t�Ĺ�ϵ���£�
?CO(g) + H2O(g)����ƽ�ⳣ���˺��¶�t�Ĺ�ϵ���£�
t��
| 700
| 800
| 850
| 1000
| 1200
|
K
| 2.6
| 1.7
| 1.0
| 0.9
| 0.6
|
(1) K�ı���ʽΪ����?��?�������÷�Ӧ������ӦΪ����?����Ӧ�������ȡ����ȡ���
(2) ���жϸ÷�Ӧ�Ƿ��Ѿ��ﵽ��ѧƽ��״̬���ǣ�?
����������ѹǿ���䡡��?�£����������COŨ�Ȳ���
�ã�v(H2)��= v(H2O)�桡��? D��c(CO2) = c(CO)��
��3��ij�о�С�����÷�Ӧ��CO(g)+H2O(g)  ?H2(g)+CO2(g) ?��H=��41.2kJ/mol���Ʊ�CO2��H2�Ļ�����塣�ü�Һ����һ����CO2�ķ�������������H2��CO2������ȡ�����1L1.5mol/L��NaOH��Һ���������22.4L��������Ϊ��״���������CO2�������պ���Һ�и�����Ũ�ȴӴ�С��˳����?��
?H2(g)+CO2(g) ?��H=��41.2kJ/mol���Ʊ�CO2��H2�Ļ�����塣�ü�Һ����һ����CO2�ķ�������������H2��CO2������ȡ�����1L1.5mol/L��NaOH��Һ���������22.4L��������Ϊ��״���������CO2�������պ���Һ�и�����Ũ�ȴӴ�С��˳����?��
��4���罫H2��CO2��4:1������Ȼ�ϣ����ʵ��������¿��Ƶ�CH4����֪��
CH4 (g) + 2O2(g)  ?CO2(g)+ 2H2O��1��?��H1����890.3 kJ/mol?
?CO2(g)+ 2H2O��1��?��H1����890.3 kJ/mol?
H2(g) + 1/2O2(g)  ?H2O��1��?��H2����285.8 kJ/mol?
?H2O��1��?��H2����285.8 kJ/mol?
��CO2(g)��H2(g)��Ӧ����CH4(g)��Һ̬ˮ���Ȼ�ѧ����ʽ��?��
��5��������ȼ�ϵ������ͼ��
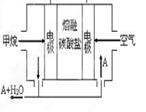
��ͼ��������̼����Ϊ����ʣ���CH4Ϊȼ�ϣ�����Ϊ��������ϡ����������Ϊ�缫����֪�����ĵ缫��Ӧ��CH4 +4CO32����8e��=5CO2+2H2O�������ĵ缫��Ӧ��_______?��Ϊ��ʹ��ȼ�ϵ�س�ʱ���ȶ����У���صĵ�������Ӧ�����ȶ���Ϊ�˵�ع���ʱ�����в���A���ʲμ�ѭ������A���ʵĻ�ѧʽ��_________��ʵ������У���ͨ���˱�״���¿���448L�����������O2�������Ϊ20%������������ȼ�ϵ�����ı�״����CH4____________L��
�ο��𰸣���1��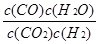 ��?���ȣ�
��?���ȣ�
��2��B��C��
��3��c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
��4��CO2(g)+4H2(g)=CH4(g)+2H2O(l) ��H=��252.9kJ/mol
��5��O2+4e-+2CO2=2CO32-?CO2?44.8
�����������1����ӦCO2(g) + H2(g)?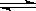 ?CO(g) + H2O(g) ƽ�ⳣ������ʽΪ
?CO(g) + H2O(g) ƽ�ⳣ������ʽΪ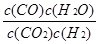 ���ɱ��������ݿ�֪�������¶����ߣ�ƽ�ⳣ�����٣�˵������Ӧ�Ƿ��ȷ�Ӧ����2�������ݻ��̶�����Ӧǰ���������ʵ������䣬����������ƽ��״̬���Ƿ�ƽ��״̬��������ѹǿ�����䣬A����ѧƽ��״̬�ı�־�������淴Ӧ������ȣ������Ũ�ȱ��ֲ��䣬����COŨ�ȱ��ֲ����״̬��ƽ��״̬��B��ȷ��H2��H2O�ļ�������Ϊ1��1������v(H2)��= v(H2O)���״̬��ƽ��״̬��C��ȷ��������̼��һ����̼Ũ����Ȳ�����Ϊ�жϷ�Ӧ��ƽ��״̬�ı�־��ƽ��ʱ����Ũ�ȿ������Ҳ���ܲ��ȣ��������̼��ʼͶ�ϺͶ�����̼��ת�����й�ϵ��D����3��CO2��NaOH��Ӧ�����������CO2+2NaOH=Na2CO3+H2O��NaOH+CO2=NaHCO3������CO2��NaOH���ʵ�����Ϊ2��3������1��1��1��2֮�䣬����1molCO2��1.5molNaOH����Na2CO3��NaHCO3����Na2CO3��NaHCO3���ʵ����ֱ�Ϊx��y����C�غ��x+y=1����Na�غ��2x+y=1.5�����x=y=0.5mol��CO32-ˮ������HCO3-��OH-��������Һ������Ũ���ɴ�С��˳��Ϊc(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)����4��CO2(g)+4H2(g)=CH4(g)+2H2O(l)? ��H=4��H2����H1����252.9 kJ/mol����5������н���Ϊ����̼���Σ�����ͨ�����������������ӦΪO2+4e-=2O2-��O2-+CO2=CO32-������ʽ��Ӽ���O2+4e-+2CO2=2CO32-���ɵ缫��Ӧ��֪ͼ�е�AΪCO2����������������ת����ȵ�CH4��8e-��2O2������ͨ���O2Ϊ4molʱ��Ӧ��CH4Ϊ2mol��
���ɱ��������ݿ�֪�������¶����ߣ�ƽ�ⳣ�����٣�˵������Ӧ�Ƿ��ȷ�Ӧ����2�������ݻ��̶�����Ӧǰ���������ʵ������䣬����������ƽ��״̬���Ƿ�ƽ��״̬��������ѹǿ�����䣬A����ѧƽ��״̬�ı�־�������淴Ӧ������ȣ������Ũ�ȱ��ֲ��䣬����COŨ�ȱ��ֲ����״̬��ƽ��״̬��B��ȷ��H2��H2O�ļ�������Ϊ1��1������v(H2)��= v(H2O)���״̬��ƽ��״̬��C��ȷ��������̼��һ����̼Ũ����Ȳ�����Ϊ�жϷ�Ӧ��ƽ��״̬�ı�־��ƽ��ʱ����Ũ�ȿ������Ҳ���ܲ��ȣ��������̼��ʼͶ�ϺͶ�����̼��ת�����й�ϵ��D����3��CO2��NaOH��Ӧ�����������CO2+2NaOH=Na2CO3+H2O��NaOH+CO2=NaHCO3������CO2��NaOH���ʵ�����Ϊ2��3������1��1��1��2֮�䣬����1molCO2��1.5molNaOH����Na2CO3��NaHCO3����Na2CO3��NaHCO3���ʵ����ֱ�Ϊx��y����C�غ��x+y=1����Na�غ��2x+y=1.5�����x=y=0.5mol��CO32-ˮ������HCO3-��OH-��������Һ������Ũ���ɴ�С��˳��Ϊc(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)����4��CO2(g)+4H2(g)=CH4(g)+2H2O(l)? ��H=4��H2����H1����252.9 kJ/mol����5������н���Ϊ����̼���Σ�����ͨ�����������������ӦΪO2+4e-=2O2-��O2-+CO2=CO32-������ʽ��Ӽ���O2+4e-+2CO2=2CO32-���ɵ缫��Ӧ��֪ͼ�е�AΪCO2����������������ת����ȵ�CH4��8e-��2O2������ͨ���O2Ϊ4molʱ��Ӧ��CH4Ϊ2mol��
���������⣨5��Ҳ����д��ȼ�ϵ���ܷ�ӦCH4+2O2=CO2+2H2O�����ܷ�Ӧ��ȥ�����缫��Ӧʽ���������缫��Ӧʽ��
�����Ѷȣ�һ��
4��ѡ���� ���ݱ�����һ��Ӳ�ijɷ�ΪCa5(PO4)3OH�����ʱ�����������Һ�д�������ƽ�⣺
Ca5(PO4)3OH 5Ca2++3 PO43��+OH������֪Ca5(PO4)3F(s)���ܽ�ȱ�a5(PO4)3OH(s)��С��Ϊ�˱������ݣ�������ؾ������˲�ͬ�Ĵ�ʩ�����´�ʩ�в��ܱ������ݵ��ǣ�?��
5Ca2++3 PO43��+OH������֪Ca5(PO4)3F(s)���ܽ�ȱ�a5(PO4)3OH(s)��С��Ϊ�˱������ݣ�������ؾ������˲�ͬ�Ĵ�ʩ�����´�ʩ�в��ܱ������ݵ��ǣ�?��
A�����ô���ˮ
B��������������������Ca2+��PO43������
C��������ˮ�м����������������Ӽ�
D���������м�����������Ӽ�
�ο��𰸣�A
���������B�����������Ca2+��PO43��������ʹƽ�����淽���ƶ���������Ca5(PO4)3OH�ķ�����У�C��D����Ǽ�������ӣ�����������Ca5(PO4)3F(s)��Ҳ�����ڱ������ݡ�
�����Ѷȣ���
5��ѡ���� 25��ʱ��ˮ�ĵ���ﵽƽ�⣺H2O H����OH������H>0������������ȷ����
H����OH������H>0������������ȷ����
A����ˮ�м���ϡ���ᣬƽ�����ƣ�c(H��)����
B����ˮ���ȣ�KW����pH����
C����ˮ�м�����������������أ�c(H��)����KW����
D��pH=10��NaOH��Һ��pH=10��NaClO��Һ�У�ˮ����c(H+)֮�ȵ���106
�ο��𰸣�C
�������������������Ũ�ȣ�����ˮ�ĵ��룬����Һ����������A����ȷ���������ȣ��¶����ߴٽ����룬��pH���ͣ�B����ȷ�������������ˮ�����ԣ�������ǿ�����¶Ȳ��䣬����ˮ�����ӻ��������䣬C��ȷ��������������ˮ�ĵ��룬��������ˮ��ٽ�ˮ�ĵ��룬����ˮ����c(H+)֮�ȵ���1�U106��D����ȷ����ѡC��
�����Ѷȣ���