1������� ��10�֣�
��1���Ʊ�������������Ļ�ѧ����ʽΪ ��
��2��̼��������ˮ��Һ�еĵ��뷽��ʽΪ ��
��3����֤��Na2SO3��Һ�д���SO32��+H2O HSO3��+OH��ˮ��ƽ�����ʵ�� ����ѡ����ĸ����
HSO3��+OH��ˮ��ƽ�����ʵ�� ����ѡ����ĸ����
A�������̪��Һ��죬�ټ���H2SO4��Һ���ɫ��ȥ
B�������̪��Һ��죬�ټ�����ˮ���ɫ��ȥ
C�������̪��Һ��죬�ټ���BaCl2��Һ����������Һ�ɫ��ȥ
��4�����п��淴Ӧ��2A(g)��2B(g) C(g)��3D(s)�����ܱ��������ݻ����¶ȶ���ͬ�������£��ֱ����������;������ƽ�⣺��. A��B����ʼ���ʵ�����Ϊ2 mol����.C��D����ʼ���ʵ����ֱ�Ϊ2 mol��6 mol������˵������ȷ���� ����ѡ����ĸ����
C(g)��3D(s)�����ܱ��������ݻ����¶ȶ���ͬ�������£��ֱ����������;������ƽ�⣺��. A��B����ʼ���ʵ�����Ϊ2 mol����.C��D����ʼ���ʵ����ֱ�Ϊ2 mol��6 mol������˵������ȷ���� ����ѡ����ĸ����
A��������;�����մﵽƽ��ʱ����ϵ�ڻ������İٷ������ͬ
B���ﵽƽ��ʱ��;�������û�����ܶ�Ϊ;�������û�����ܶȵ�2��
C���ﵽƽ��ʱ��;����C��ƽ��Ũ�ȴ���;����C��ƽ��Ũ�ȵ�2��
��5���ں��ݾ��ȣ�������罻�������������½���2A (g)+ B(g) 2C(g)+ D(s)��Ӧ�����±�����Ͷ�ϣ���Ӧ�ﵽƽ��״̬�������ϵѹǿ���ߡ������÷�Ӧ��ƽ�ⳣ�����¶ȵı仯��ϵ�� ��
2C(g)+ D(s)��Ӧ�����±�����Ͷ�ϣ���Ӧ�ﵽƽ��״̬�������ϵѹǿ���ߡ������÷�Ӧ��ƽ�ⳣ�����¶ȵı仯��ϵ�� ��
2��ѡ���� �Ƚ�������Һ��pH? (�����������������=����
(1)25�桢1mol/LFeCl3��Һ_____80�桢1mol/LFeCl3��Һ��
(2)0��1mol/L(NH4)2CO3��Һ______0��1mol/L Na2CO3��Һ��
(3)0��1mol/LNH4Cl��Һ______0��01mo1/L NH4Cl��Һ��
(4)0��1mol/LNa2CO3��Һ______0��1mol/L NaHCO3��Һ��
A.>?
B.> > > >
C.?
D.? >
3������� ��10�֣������£�������7����Һ��A.Na2CO3 B.CH3COONa C.AlCl3
D.CH3COOH E.NaHCO3 F.NaOH G.HCl��
��ش��й����⣺
��1��A��Һ�Լ��Ե����ӷ���ʽ�ǣ� ��
��2����C��Һ�������պ�õ��Ĺ����ǣ�д��ѧʽ���� ��C��E�ǡ���ĭ���������ҩƷ��д������Һ��Ϸ�Ӧ�����ӷ���ʽ�� ��
��3����A��E������Һ��pH��ͬ�����ʵ���Ũ�ȴ�С��ϵ�� ��
��4��A��B��F��Һ��25mL�����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L�����ֱ����25mL 0.1mol/L ��G��Һ��pH�����ǣ� �����A��B��F����
4��ѡ���� ��ϩ����CH2�TCHCH2OH���ɷ����Ļ�ѧ��Ӧ�У�������
��ȡ����Ӧ���ڼӳɷ�Ӧ���ۼӾ۷�Ӧ����������Ӧ��
A���٢ۢ�
B���ڢ�
C���٢ڢۢ�
D���ڢۢ�
5��ѡ���� ��NA��ʾ�����ӵ�������ֵ������˵������ȷ��
��һ�������¶��������г���3molH2(g)��1molN2(g)������Ӧ��3H2(g)+N2(g)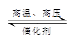 2NH3(g)����H=-QkJ/mol�����÷�Ӧ�ų�0��25QkJ������ʱ�������е������������2��25NA
2NH3(g)����H=-QkJ/mol�����÷�Ӧ�ų�0��25QkJ������ʱ�������е������������2��25NA
�ڳ����£�21gC3H6��C4H8�Ļ�����к��е�̼ԭ����Ϊ1��5NA
��14��2g�����ƹ����к���0��1NA�������Ʒ��ӣ�
��2gD216O�к��е�������?������?��������ΪNA
�ݱ�״���£�11��2L�ȷ��к���C-Cl������ĿΪ1��5NA
��100mL0��1mol��L-1��FeCl3��Һ�����ˮ�п��Ƶ�Fe(OH)3����0��01NA
A���٢ۢ�
B���ܢݢ�
C���٢ڢ�
D���٢�