1、选择题 25℃时,有c(CH3COOH)+c(CH3COO-)=0.1mol/L的一组醋酸、醋酸钠混合溶液,溶液中
c(CH3COOH)、c(CH3COO-)与pH的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是
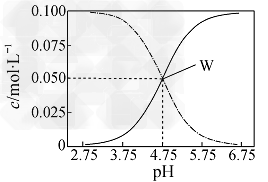
[? ]
A.pH=5.5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-)
C.pH=3.5的溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol・L-1
D.向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-)
参考答案:BC
本题解析:
本题难度:一般
2、选择题 下列溶液中微粒的物质的量浓度关系正确的是
[? ]
A.室温下,向0. 01mol・L-1 NH4HSO4溶液中滴加NaOH溶液至中性:
c(Na+)>c(SO42-)> c(NH4+)>c(OH-)=c(H+)
B.0. 1mol・L-1NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+)
C.Na2CO3溶液:c(OH-) -c( H+) =c(HCO3-)+2c(H2CO3)
D.25℃时,pH=4.75、浓度均为0.1mol・L-1的CH3COOH、CH3COONa混合溶液:
c(CH3COO-)+ c(OH-)<c(CH3COOH)+c(H+)
参考答案:AC
本题解析:
本题难度:一般
3、选择题 某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法正确的是
[? ]
A.若c(OH-)>c(H+),溶液中不可能存在:c(Na+)>c(OH-)>c(A-)>c(H+)
B.溶液中不可能存在:c(Na+)>c (A-)>c(OH-)>c(H+)
C.若溶液中c(A-) = c(Na+),则溶液一定呈中性
D.若溶质为NaA、HA,则一定存在:c(A-)>c(Na+)>c(H+)>c(OH-)
参考答案:C
本题解析:
本题难度:一般
4、简答题 现有浓度均为0.1mol?L-1的下列溶液:
①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水.
请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)______.
(2)④、⑤、⑥、⑦四种溶液中NH4+浓度由大到小的顺序是(填序号)______.
(3)将③和④按体积比1:2混合后,混合液中各离子浓度由大到小的顺序是______.
(4)已知t℃时,KW=1×10-13,则t℃(填“>”、“<”或“=”)______25℃.在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a:b=______.
(5)同体积、同物质的量浓度的①硫酸和②醋酸溶液,分别用同浓度的NaOH溶液完全中和,所需NaOH体积大小关系为①______②(填“>”、“<”或“=”).
(6)同体积、相同PH的①硫酸和②醋酸溶液中分别投入足量且等质量的锌,开始放H2的速率:①______②,片刻后①______②,到反应结束,所用时间①______②.
参考答案:(1)酸或碱抑制水电离,含有弱离子的盐促进水电离,酸中氢离子浓度或碱中氢氧根离子浓度越大其抑制水电离程度越大,0.1mol/L的①硫酸、②醋酸、③氢氧化钠、④氯化铵中,硫酸中氢离子浓度为0.2mol/L、醋酸中氢离子浓度小于0.1mol/L、氢氧化钠溶液中氢氧根离子浓度为0.1mol/L,氯化铵促进水电离,所以①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是④②③①,故答案为:④②③①;
(2)氯化铵、醋酸铵、硫酸氢铵属于强碱,在水溶液里完全电离,一水合氨是弱电解质,在水溶液里部分电离,醋酸根离子促进铵根离子水解、氢离子抑制铵根离子水解,所以铵根离子浓度大小顺序是⑥④⑤⑦,故答案为:⑥④⑤⑦;
(3)将③和④按体积比1:2混合后,溶液中的溶质是等物质的量浓度的NaCl、NH4Cl、NH3.H2O,一水合氨的电离程度大于铵根离子水解程度,所以溶液呈碱性,一水合氨电离导致溶液中c(NH4+)>c(Na+),结合物料守恒、溶液酸碱性知,溶液中离子浓度大小顺序是c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),
故答案为:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+);
(4)水的电离是吸热反应,升高温度促进水电离,在水的离子积常数增大,t℃时,KW=1×10-13,则t℃>25℃,t℃时将pH=11的NaOH溶液中c(OH-)=10-1310-11mol/L=0.01mol/L,
pH=1的H2SO4溶液中c(H+)=0.1mol/L,混合溶液中c(H+)=0.1b-0.01aa+bmol/L=0.01mol/L,则a:b=9:2,
故答案为:>;9:2;
(5)物质的量相等的硫酸和醋酸,分别用同浓度的NaOH溶液完全中和,所需NaOH体积大小与酸的元数成正比,硫酸是二元酸、醋酸是一元酸,所以所需NaOH体积大小关系为①>②,故答案为:>;
(6)pH相等的醋酸和硫酸溶液中,生成氢气的速率与氢离子浓度成正比,氢离子浓度相等则其反应速率相等,所以pH相等的醋酸和硫酸中开始反应速率相等;
随着反应的进行,硫酸中氢离子浓度减少,醋酸电离出氢离子导致醋酸中氢离子浓度大于硫酸,则反应速率为①<②;
硫酸的反应速率小于醋酸,所以反应时间①>②,
故答案为:=;<;>.
本题解析:
本题难度:简单
5、选择题 有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①CH3COONa与HCl;?
②CH3COONa与NaOH?③CH3COONa与NaCl?④CH3COONa与NaHCO3,下列各项排序正确的是
[? ]
A.pH:②>③>④>①?
B.c(CH3COOH):①>④>③>②
C.c(CH3COO-):②>④>③>①?
D.溶液中c(H+):①>③>②>④
参考答案:C
本题解析:
本题难度:一般