1��ѡ���� ̼����(SiC)��һ�־���������ƽ��ʯ�Ľṹ������̼ԭ�Ӻ�ԭ�ӵ�λ���ǽ���ġ����������־���ٽ��ʯ���ھ���衢��̼�����У����ǵ��۵�Ӹߵ��͵�˳����
[ ? ]
A���٢ۢ�
B���ڢۢ�
C���ۢ٢�
D���ڢ٢�
�ο��𰸣�A
���������
�����Ѷȣ�һ��
2��ѡ���� ���з��ӻ������У����ṩ�¶Ե�����ijЩ���������γ���λ������
[? ]
��H2O ��NH3 ��F- ��CN- ��CO
A.�٢�
B.�٢ڢ�
C.�٢ڢ�
D.�٢ڢۢܢ�
�ο��𰸣�D
���������
�����Ѷȣ���
3��ѡ���� �����йػ�ѧ����ʹ����ȷ����
[? ]
A����ԭ�ӵ�ԭ�ӽṹʾ��ͼ��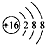
B��NH4Cl�ĵ���ʽ��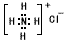
C��ԭ�Ӻ�����10�����ӵ���ԭ�ӣ�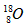
D�����ȼױ��Ľṹ��ʽ��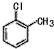
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� �̿�ѧ�ҷ���C3O2�ǽ��Ǵ����ɷ�֮��2004�꣬������ѧ��ͨ������������̫�ճ�̽���ˮ�Ǵ����к���һ�ֳ�Ϊ���ʣ���ѧʽΪCOS�������ʣ���֪�����������̼�Ľṹ���ƣ����������л�ȼ�գ������й�C3O2�����ʵ�˵������ȷ���� ��������
A��C3O2��������������ȫȼ������CO2
B��C3O2��CO2����̼����������ǻ�Ϊͬ���칹��
C��COS���ɼ��Լ����ɵķǼ��Է��ӣ�����������ԭ�Ӷ�����8�����ȶ��ṹ
D��COS����������ȫȼ�պ���������CO2��SO3��
�ο��𰸣�A��C3O2��C�Ļ��ϼ�Ϊ+43�������̬�����л�ԭ�ԣ��ܱ������������ɶ�����̼����A��ȷ��
B��C3O2��CO2����̼������������Ƿ���ʽ��ͬ�����Բ���ͬ���칹�壬��B����
C����ΪCOS������������IJ��غϣ�����COS���ɼ��Լ����ɵļ��Է��ӣ�������������ԭ�Ӷ�����8�����ȶ��ṹ����C����
D��COS����������ȫȼ������CO2��SO2��SO2��O2��Ӧ���ڴ��������²�������SO3����D����
��ѡA��
���������
�����Ѷȣ���
5������� �����ʽṹ�����ʡ���8�֣�
��ɵ����ʵ�Ԫ����Ҫ��C��H��O��N��S��P��������Cu��Fe��Zn�ȣ�����ͭ����Ͻ�����������ʹ�õĽ������ϣ���;�㷺��
��1��ͭԭ�ӵĺ�������Ų�ʽ��??��O��N��S�ĵ�һ�������ɴ�С��˳��Ϊ?��
��2��ͭ���۵�ȸƸߣ���ԭ����?��
��ͼ�ǽ���Ca��Cu���γɵ�ij�ֺϽ�ľ����ṹʾ��ͼ����úϽ���Ca��Cu��ԭ�Ӹ�����Ϊ?��

��3��Cu2+����NH3��H2O��Cl-���γ���λ��Ϊ4������
��[Cu��NH3��4]2+�д��ڵĻ�ѧ��������?������ţ���
A����λ��B��������C�����Թ��ۼ�D���Ǽ��Թ��ۼ�E�����Ӽ�
��[Cu��NH3��4]2+���жԳƵĿռ乹�ͣ�[Cu��NH3��4]2+�е�����NH3������Cl-ȡ�����ܵõ����ֲ�ͬ�ṹ�IJ����[Cu��NH3��4]2+�Ŀռ乹��Ϊ?������ţ���
A��ƽ��������? B����������? C��������? D��V��
��ij�ֺ�Cu2+�Ļ�����ɴ���ϩ���Ʊ���ȩ�ķ�Ӧ��
HOCH2CH=CH2��CH3CH2CHO���ڱ�ϩ�������з���ij�ַ�ʽ�ӻ���̼ԭ�����DZ�ȩ�����з���ͬ����ʽ�ӻ���̼ԭ������2����������̼ԭ�ӵ��ӻ���ʽΪ?��
�ο��𰸣���1��1s22s22p63s23p63d104s1 ��1�֣�N��O��S ��1�֣�
(2)������ͭ�Ľ�����ǿ�ڸ�?��2�֣�? 1��5��1�֣�
��3����AC?��1�֣�? ��A?��1�֣�? ��sp2�ӻ���1�֣�
���������
��1��ͭԭ�ӵĺ�������Ų�ʽ��1s22s22p63s23p63d104s1��O��N��S�ĵ�һ�������ɴ�С��˳��ΪN��O��S��Nԭ�ӵ�2P3Ϊ������ṹ�����ȶ�����һ�����ܴ���ͬ���ڵ���ԭ�ӡ�
��2��ͭ���۵�ȸƸߣ�ͭ���ǽ������壬˵��ͭ�Ľ�����ǿ�ڸƣ���ԭ�ӣ�8��1/8=1,ͭ��
8��1/2+1=5��
��3����[Cu��NH3��4]2+�д��ڵĻ�ѧ�����ͣ�Cu2�� ��NH3����֮����λ����NH3��N�DH�����Թ��ۼ�����ѡAC��
��������������壬����NH3������Cl-ȡ����ṹ��ͬ��A��ȷ��
��HOCH2CH=CH2������SP2һ��SP3, CH3CH2CHO��2��SP3��1��SP2, �ڱ�ϩ�������з���ij�ַ�ʽ�ӻ���̼ԭ�����DZ�ȩ�����з���ͬ����ʽ�ӻ���̼ԭ������2����������̼ԭ�ӵ��ӻ���ʽΪsp2�ӻ�.
�����Ѷȣ�һ��