1、选择题 下列反应的离子方程式中正确的是( )
A.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应 CH3OH+H2O-6e-=CO2↑+6H+
B.在NaHSO4溶液中加Ba(OH)2至中性 H++SO42-+Ba2++O来源:91exam .orgH-=BaSO4↓+H2O
C.苯酚钠的水溶液中通入少量的CO2 2C6H5O?+CO2+H2O→2C6H5OH+CO32-
D.用侯氏制碱法制得NaHCO3 Na++NH3+CO2+H2O=NaHCO3↓+NH4+
2、选择题 某粗盐中含有Ca2+、Mg2+、SO42-等杂质,现测定氯化钠含量.取120g粗盐溶于水过滤除去6g不溶物,向滤液中依次加入过量的下列试剂:1mol/L的氢氧化钠溶液200mL、4.56g固体氯化钡、31.8%的碳酸钠溶液10g,发现白色沉淀逐渐增多,过滤除去沉淀物,再往滤液中加入过量的盐酸,使溶液呈酸性,加热蒸发得氯化钠晶体126.65g,则粗盐中含氯化钠的质量分数为( )
A.94.1%
B.92.9%
C.86.3%
D.83.2%
3、选择题 下列离子方程式中,正确的是
A.Na2O2与H2O反应制备O2:Na2O2 + H2O= 2Na+ + 2OH- + O2↑
B.向稀硝酸中加入少量铁粉:3Fe + 8H+ + 2NO3-= 3Fe2+ + 2NO↑ + 4H2O
C.氯化镁溶液与氨水反应:Mg2+ + 2OH-=Mg(OH)2↓
D.向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42―+2Ba2++4OH―=2BaSO4↓+AlO2―+2H2O
4、填空题 亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:

已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体只能保持在稀释状态下以防止爆炸性分解,且需现合成现用。
③ClO2气体在中性和碱性溶液中不能稳定存在。
(1)在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,请写出阳极的电极反应方程式:?。
(2)反应生成ClO2气体需要X酸酸化的原因为:?。X酸为?。
(3)吸收塔内的温度不能过高的原因为:?
(4)吸收塔内ClO2随着还原剂的不同和溶液酸碱性的变化可被还原为ClO2―或Cl―。ClO2被S2―还原为ClO2―、Cl―的转化率与溶液pH的关系如右图所示。
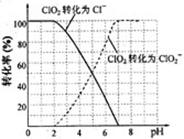
请写出pH≤2时ClO2与S2―反应的离子方程式:?。
(5)第二步向NaClO3溶液中通SO2的同时通入空气的原因为:?。
(6)从滤液中得到NaClO2●3H2O粗晶体的操作步骤为
?、?、?。
5、简答题 写出下列反应的离子方程式:
(1)Fe2(SO4)3溶液中加入氢氧化钠溶液______
(2)用食醋除去热水瓶胆内壁的水垢(主要成分为CaCO3)______
(3)氢氧化镁溶于稀硝酸中______
(4)碳酸氢钙溶液中加入足量稀盐酸______.