1、选择题 下列关于性质递变规律的叙述不正确的是( )
A.还原性:Na>Mg>Al>S
B.氧化性:F>Cl>S>P
C.酸性:H2CO3<H3PO4<H2SO4<HClO
D.稳定性:SiH4<PH3<NH3<H2O
参考答案:A、Na、Mg、Al、S为同周期元素,从左向右金属性减弱,则还原性为Na>Mg>Al>S,故A正确;
B、同周期元素,从左向右非金属性增强,则Cl>S>P,同主族从上到下非金属性减弱,则氧化性F>Cl>S>P,故B正确;
C、HClO为弱酸,非金属性越强,最高价氧化物对应水化物的酸性为H2CO3<H3PO4<H2SO4<HClO4,,故C错误;
D、非金属性O>N>P>Si,对应的气态氢化物稳定性为SiH4<PH3<NH3<H2O,故D正确;
故选C.
本题解析:
本题难度:简单
2、选择题 如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是
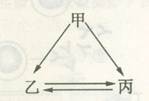
①C;②H2O2;③Na;④Fe;⑤HNO3
A.仅①③④
B.仅①②⑤
C.仅①②③⑤
D.①②③④⑤
参考答案:D
本题解析:运用代入法进行判断①若甲是C,与O2反应可能生成CO或CO2,则乙、丙分别为CO、CO2,CO与O2反应可生成CO2,CO2与C反应可生成CO,正确;②若甲是H2O2,H2O2分解可得H2O和O2,则乙、丙分别为H2O、O2,H2O电解可得O2,O2与H2反应可得H2O,正确;③若甲是Na,钠与Cl2反应可生成NaCl,Na与H2O反应可生成NaOH,则乙、丙可能是NaCl、NaOH,NaOH与HCl反应可生成NaCl,用惰性电极电解NaCl溶液可生成NaOH,正确;④若甲是Fe,Fe在Cl2中燃烧生成FeCl3,Fe与HCl反应可生成FeCl2,则乙、丙可能是FeCl2、FeCl3,FeCl2与Cl2反应生成FeCl3,FeCl3与Fe反应可生成FeCl2,正确;⑤若甲为HNO3,HNO3与Cu反应可生成NO或NO2,则乙、丙可能是NO、NO2,NO与O2反应生成NO2,NO2与H2O反应生成NO,正确,故D项正确。
本题难度:一般
3、选择题 元素的周期数等于?
[? ]
A.?电子层数?
B.?原子量?
C.?次外层电子数?
D.?最外层电子数
参考答案:A
本题解析:
本题难度:简单
4、选择题 已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E 的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是
[? ]
A.元素A、B组成的化合物常温下一定呈气态
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
C.工业上常用电解法制备元素C、D、E的单质
D.化合物AE与CE含有相同类型的化学键
参考答案:BC
本题解析:
本题难度:一般
5、选择题 已知下列序号的元素为金属元素,其中属于稀土金属元素的是
[? ]
A.20号?
B.31号
C.69号?
D.114号
参考答案:C
本题解析:
本题难度:简单