1、选择题 体积为1升的干燥容器中充人HC1气体后,测得容器中气体对氧气的相对密度为1.082。将此气体倒扣在水中,最终进入容器中液体的体积是
[?]
A.0.25 L
B.0.5 L
C.0.75 L
D.1L
2、选择题 将a?mol纯铁粉投入含HNO3?b?mol的稀溶液里,恰好完全反应并放出NO气体,则a和b的关系是
[? ]
A.a/b=1/4?
B.a/b=3/8
C.1/4≤a/b≤3/8?
D.a/b的值无法确定
3、选择题 下图表示金属X、 Y以及它们的合金Z分别与足量盐酸反应时产生氢气的情况,其中横坐标表示消耗金属的物质的量,纵坐标表示产物氢气的体积(标准状况)。 下列对有关Z的组成的判断,正确的是
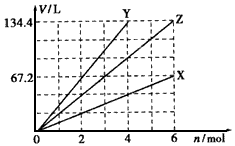
[? ]
A.n(Na) : n(Fe)=2:1
B.n(Mg):n(K)=1:2
C.n(Na) : n(Al) =1:3
D.n(K):n(Al)=1:1
4、选择题 两份铝屑,第一份与足量的稀盐酸反应,第二份与足量的氢氧化钠溶液反应,产生氢气的体积比为1:2(同温同压下),则两份铝屑的质量比为
[? ]
A.1:1
B.1:2
C.1:3
D.1:4
5、计算题 已知达喜是常用的中和胃酸的药物,其化学成分是铝和镁的碱式盐。
(1)取该碱式盐3.01?g,加入2.0?mol/L盐酸使其溶解,当加入盐酸42.5?mL时开始产生CO2,加入盐酸至45.0?mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比。
(2)在上述碱式盐溶于盐酸后的溶液中加入过量氢氧化钠,过滤,沉淀物进行干燥后重1.74?g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的化学式。