1、选择题 已知:合成氨是一个放热反应,下列事实不能用勒沙特列原理来解释的是( )
A.加压有利于SO2与O2反应生成S03
B.500℃左右比常温下更有利于合成氨
C.将混合气中的氨气液化,有利于合成氨的反应
D.用过量空气煅烧硫铁矿可以提高原料的利用率
参考答案:A.存在平衡2SO2+O2(g)?2SO3(g),正反应为气体体积减小的反应,增大压强,平衡向正反应移动,有利于合成SO3,能用勒沙特列原理解释,故A不选;
B.存在平衡2N2+3H2?2NH3,合成氨是放热过程,高温不利于氨气的合成,选择500℃考虑反应速率较快、且催化剂活性较高,故B选;
C.氨气液化,氨气的浓度降低,平衡向合成氨的方向移动,能用勒沙特列原理解释,故C不选;
D.过量空气煅烧硫铁矿,增大氧气的浓度,有利于反应向生成二氧化硫的方向移动,可以提高原料,能用勒沙特列原理解释,故D不选;
故选B.
本题解析:
本题难度:一般
2、填空题 在固定容积的密闭容器中,有可逆反应nA(g)+mB(g)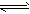 pC(g)处于平衡状态(已知n+m>p,△H>0)。完成以下问题(填写:增大、减小、不变、不确定)
pC(g)处于平衡状态(已知n+m>p,△H>0)。完成以下问题(填写:增大、减小、不变、不确定)
(1)升高温度时c(B)/c(C)的比值__________,混合气体的密度____________;
(2)降温时,混合气体的平均相对分子质量___________;
(3)加入催化剂,气体的总物质的量___________;
(4)充入C,则A、B的物质的量____________。
参考答案:(1)减小;不变
(2)减小
(3)不变
(4)增大
本题解析:
本题难度:一般
3、选择题 常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两个实验:(N2O4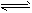 2NO2 △H > 0)(a)将两容器置于沸水中加热(b)在活塞上都加2kg的砝码在以上两情况下,甲和乙容器的体积大小的比较,正确的是
2NO2 △H > 0)(a)将两容器置于沸水中加热(b)在活塞上都加2kg的砝码在以上两情况下,甲和乙容器的体积大小的比较,正确的是

[? ]
A.(a)甲>乙,(b)甲>乙
B.(a)甲>乙,(b)甲=乙
C.(a)甲<乙,(b)甲>乙
D.(a)甲>乙,(b)甲<乙
参考答案:D
本题解析:
本题难度:一般
4、填空题 现有反应:mA(g)+nB(g)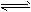 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则
(1)该反应的逆反应为_________热反应,且m+n_________p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率_________,B的转化率_________。
(4)若升高温度,则平衡时B、C的浓度之比_________。
(5)若加入催化剂,平衡时气体混合物的总物质的量_________。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______,而维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
参考答案:(1)放;>
(2)增大
(3)增大;减小
(4)变小
(5)不变
(6)变深;变浅
本题解析:
本题难度:一般
5、选择题 已知反应2SO2(g)+O2(g)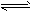 2SO3(g)ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入
2SO3(g)ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入
SO2和O2,在一定条件下发生反应。下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是
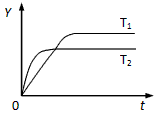
[? ]
A.O2的体积分数
B.混合气体的密度
C.密闭容器内的压强
D.SO2的转化率
参考答案:D
本题解析:
本题难度:一般