1、选择题 用NA表示阿伏加德罗常数,下列说法正确的是
[? ]
A.0.2 mol H2O2完全分解转移的电子数为0.4 NA
B.1molCl2与1mol Fe反应,转移的电子数为3NA
C.在标准状况下,Cl2和H2的混合气22.4L,光照后原子总数为2NA
D.在常温常压下,2.24 L SO2与O2混合气体中所含氧原子数为0.2 NA
参考答案:C
本题解析:
本题难度:简单
2、选择题 NA表示阿伏加德罗常数,下列判断正确的是
[? ]
A.在18 g18O2中含有NA个氧原子
B.标准状况下,22.4L空气含有NA个单质分子
C.等物质的量的N2和CO所含分子数均为NA
D.1.7g H2O2中含有的电子数为0.9NA
参考答案:AD
本题解析:
本题难度:简单
3、选择题 设NA为阿伏加德罗常数值,下列说法中正确的是( )
A.氧化还原反应中,若消耗7.1gCl2,必转移0.2NA个电子
B.25℃,1.01×105Pa,64gS02中含有的原子数为3NA
C.NA个一氧化碳分子和0.5mol甲烷(CH4)的质量比为7:4
D.标准状况下,11.2L氦气所含的原子数为NA
参考答案:A、7.1g氯气的物质的量为1mol.氯气与金属单质的反应,1mol氯气转移2mol电子;氯气与氢氧化钠溶液的反应,1mol氯气转移了1mol电子,所以氯气参加的氧化还原反应中,若消耗7.1g Cl2,转移的电子数不一定为0.2NA,故A错误;
B、64g二氧化硫的物质的量为1mol,含有3mol原子,含有的原子数为3NA,故B正确;
C、NA个一氧化碳分子的物质的量为1mol,质量为28g;0.5mol甲烷(CH4)的质量为8g,二者质量之比为28:8=7:2,故C错误;
D、标准状况下,11.2L氦气的物质的量为0.5mol,含有0.5mol氦原子,所含的原子数为0.5NA,故D错误;
故选B.
本题解析:
本题难度:简单
4、选择题 用NA表示阿伏加德罗常数,下列叙述中不正确的是( )
A.在标准状况下,NA个甲基(-CH3)和NA个羟基(-OH)所含电子数相等
B.1mol苯中含有3NA个碳碳双键
C.46gNO2和N2O4混合气体中含有的原子总数为3NA
D.用含4molHCl的浓盐酸跟足量二氧化锰反应,生成的氯气在标准状况下的体积小于22.4L
参考答案:解;A、NA个甲基(-CH3)为1mmol,所含电子数9mol,NA个羟基(-OH)为1mol,含电子数9mol,故A正确;
B、苯分子中不含碳碳双键,故B错误;
C、46gNO2和N2O4混合气体中所含原子数可以计算46gNO2中所含原子=46g46g/mol×3=3mol,故C正确;
D、用含4molHCl的浓盐酸跟足量二氧化锰反应,浓盐酸随着反应进行变为稀盐酸后不再与二氧化锰反应,所以生成的氯气在标准状况下的体积小于22.4L,故D正确;
故选B.
本题解析:
本题难度:简单
5、选择题 某固态非金属单质A和氧气发生化合反应生成B(B为气体),在同温同压的条件下,气体B的体积是反应掉氧气体积的两倍.以下对B的分子组成的推测一定正确的是
A.有1个氧原子
B.有2个氧原子
C.有1个A原子
D.有2个A原子
参考答案:A
本题解析:分析:同温同压下气体的Vm相同,根据n=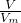 结合质量守恒定律进行判断.
结合质量守恒定律进行判断.
解答:同温同压下气体的Vm相同,由n=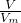 可知,气体的体积之比等于物质的量之比,则有1molO2可生成2molB,
可知,气体的体积之比等于物质的量之比,则有1molO2可生成2molB,
则B中应含有1个O,
故选A.
点评:本题考查阿伏加德罗定律及其推论,题目难度不大,注意质量守恒定律的应用.
本题难度:一般