1��ѡ���� ��a g���ۼ������NaOH��Һ�г�ַ�Ӧ��������ȫ�ܽ⣬���ռ�����״����b L������������Һ�й���c���������ӣ���Ӧ��ת�Ƶ���d�������ӵ�������NA���ɱ�ʾΪ
A��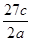
B��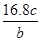
C��
D��
�ο��𰸣�C
������������������ʵ����� ��ת�Ƶ��ӵ����ʵ�����
��ת�Ƶ��ӵ����ʵ����� ���������ӵ�������NA���ɱ�ʾΪ
���������ӵ�������NA���ɱ�ʾΪ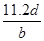 ���������ʵ�����
���������ʵ�����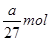 ��ת�Ƶ��ӵ����ʵ�����
��ת�Ƶ��ӵ����ʵ�����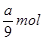 ���������ӵ�������NA���ɱ�ʾΪ
���������ӵ�������NA���ɱ�ʾΪ ��C��ȷ��������Һ�����ʼ����������ƣ�����ƫ�����ƣ�������c��ʾ�����Դ�ѡC��
��C��ȷ��������Һ�����ʼ����������ƣ�����ƫ�����ƣ�������c��ʾ�����Դ�ѡC��
����������Ĺؼ�����ȷ��Ӧ��ԭ�����Լ��������밢���ӵ������Ĺ�ϵ����ν������������ü��ɣ�����������ѧ���������������ͳ���˼ά���������ѧ����Ӧ��������
�����Ѷȣ�һ��
2��ѡ���� �������ʼ��ÿ��ת��ͨ��һ����Ӧ����ʵ�ֵ��ǣ�������
A��Al��Al2O3��Al��OH��3��NaAlO2
B��Fe��FeCl2��Fe��OH��2��Fe��OH��3
C��S��SO3��H2SO4��MgSO4
D��Si��SiO2��H2SiO3
�ο��𰸣�A��Al2O3���������ᷴӦ����Al3+��Ȼ����Ӧ����Al��OH��3������һ��ʵ�֣���A����
B���������ᷴӦ�����Ȼ��������Ȼ�������Ӧ������������������������������������Ϊ����������ÿ��ת������һ����Ӧʵ�֣���B��ȷ��
C��S��SO3��ת����Ӧ������������Ӧ���ɶ�����������������������Ӧ����������������ֱ�ӷ�Ӧ������������C����
D���������費����ˮ��Ӧ���ɹ��ᣬ�������������������Ʒ�Ӧ���ɹ����ƣ������������ᷴӦ���ɹ��ᣬ��D����
��ѡB��
���������
�����Ѷȣ�һ��
3������� ��15.6gNa2O2��2.7gA1�ۻ�Ϻ�Ͷ��������ˮ�У���ַ�Ӧ��û�ܲ���������ȫ���ų�����
��1��Na2O2��ˮ��Ӧ�����ӷ���ʽΪ______��
15.6gNa2O2�ڸ÷�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ______��
��2����Ӧ����ʱ�������������ڱ�״����Ϊ______��
��3��ȡagNa2O2��Al����ɵĻ�������������ˮ�У�������ȫ�ܽ⣬�ڱ�״���·ų���������ΪVL����V��ȡֵ��Χ��______���ú�a�Ĵ���ʽ��ʾ������ɲ�����
�ο��𰸣���1������������ˮ��Ӧ����������������������Ӧ���ӷ���ʽΪ2Na2O2+2H2O=4N+a+4OH-+O2����
15.6gNa2O2�����ʵ���Ϊ15.6g78g/mol=0.2mol������������ȫ��Ӧ����Ӧ�й�������������������ԭ�����ã���ռ12��
ת�Ƶ�����Ϊ0.2mol��12��2=0.2mol��
�ʴ�Ϊ��2Na2O2+2H2O=4N+a+4OH-+O2����0.2mol��
��2��15.6gNa2O2�����ʵ���Ϊ15.6g78g/mol=0.2mol�������ɵ��������Ƶ����ʵ���Ϊxmol������Ϊymol����
? 2Na2O2+2H2O�T4NaOH+O2����
? 2? 4? 1
? 0.2mol?xmol? ymol
����x=0.4��y=0.1��
2.7gA1�۵����ʵ���Ϊ0.1mol���ɷ���ʽ2Al+2NaOH+2H2O�T2NaAlO2+3H2����֪��0.1mol����ȫ��Ӧ��Ҫ��������0.1mol������ȫ��Ӧ��������Ӧ��������zmol����
2Al+2NaOH+2H2O�T2NaAlO2+3H2��
2? 3
0.1mol? zmol
����z=0.15��
�����ڱ�״���·�Ӧ����ʱ������������Ϊ��0.1mol+0.15mol����22.4L/mol=5.6L��
�ʴ�Ϊ��5.6L��
��3����Al��Na2O2��ˮ��Ӧ���ɵ�NaOHǡ�÷�Ӧ�����ݷ�Ӧ2Na2O2+2H2O�T4NaOH+O2����2Al+2NaOH+2H2O�T2NaAlO2+3H2����֪���������Ƶ����ʵ��������ӵ����ʵ���֮�ȵ���1��2����������Ƶ����ʵ���Ϊxmol������Ϊ2xmol������78x+54x=a�����x=a132��������������Ϊ��
?2Na2O2+2H2O�T4NaOH+O2����
?2? ?1?
? a132?mol?12��a132mol?
?2Al+2NaOH+2H2O�T2NaAlO2+3H2����
?2? 3
2��a132mol?3��a132mol
�������ɵ��������Ϊ��12��a132mol+3��a132mol����22.4L/mol=156.8a264L��
��ֻ�й������ƣ�ag�������Ƶ����ʵ���Ϊag78g/molo=a78mol����������Ϊ��
2Na2O2+2H2O�T4NaOH+O2��
?2? ?1?
a78mol?12��a78mol
���������������Ϊ?12��a78mol��22.4L/mol=22.4a156L��
�����������V��ȡֵ��ΧΪ22.4a156��V��156.8a264��
�ʴ�Ϊ��22.4a156��V��156.8a264��
���������
�����Ѷȣ�һ��
4��ѡ���� ���� ��(Be)���仯����������ƵĻ�ѧ���ʣ������Ȼ�������ڼ�����ͬ�������Ȼ��ᄃ����۵㶼�ϵ͡���֪��Ӧ��BeCl2+Na2BeO2+2H2O��2NaCl+2Be(OH)2������ȫ���У��������ƶ���ȷ����
��(Be)���仯����������ƵĻ�ѧ���ʣ������Ȼ�������ڼ�����ͬ�������Ȼ��ᄃ����۵㶼�ϵ͡���֪��Ӧ��BeCl2+Na2BeO2+2H2O��2NaCl+2Be(OH)2������ȫ���У��������ƶ���ȷ����
A��Na2BeO2��Һ��pH>7���������ɲ����պ�õ��IJ�����ΪBeO
B��BeCl2��Һ��pH<7���������ɲ����պ�õ��IJ����������BeO
C��Be(OH)2�����������ᣬ��������NaOH��Һ
D��BeCl2ˮ��Һ�ĵ�����ǿ����BeCl2�����ӻ�����
�ο��𰸣�BC
�����������
�����Ѷȣ���
5��ѡ���� ���Ƶ�˼ά�����ڻ�ѧѧϰ���о��о����õ�������ʱ���������Ľ��ۡ���ˣ��Ƴ��Ľ�������Ҫ����ʵ���ļ�����ܾ������Ƿ���ȷ�����¼������ƽ����У�����ȷ����
[? ]
A������þʧ�����ö�����̼�������𣻽�����ʧ��Ҳ�����ö�����̼��𡡡�
B��Fe3O4����д��FeO��Fe2O3��Pb3O4Ҳ����д��PbO��Pb2O3 ����
C�������õ��AlCl3��Һ����ȡ��������Ҳ�����õ��MgCl2��Һ����ȡ����þ����
D��Al��Sֱ�ӻ���ʱ�ɵõ�Al2S3��Fe��Sֱ�ӻ���ʱҲ�ɵõ�Fe2S3
�ο��𰸣�BD
���������
�����Ѷȣ�һ��