1、选择题 下列离子方程式书写不正确的是
A.氯水和碘化钾反应:Cl2+ 2I― =2Cl― + I2
B.二氧化锰和盐酸制氯气:MnO2 + 4H+ + 2Cl― =Mn2++ Cl2↑+ 2H2O
C.氢氧化钙溶液吸收氯气:Cl2 + 2OH― =Cl― + ClO― + H2O
D.氯气和水反应:Cl2 + H2O=2H+ +Cl― + ClO―
参考答案:D
本题解析:氯气与水反应生成盐酸和次氯酸,次氯酸属于弱酸不能拆开D错误。
本题难度:一般
2、选择题 能正确表示下列化学反应的离子方程式是( )
A.金属铝溶于盐酸中:Al+2H+=Al3++H2↑
B.碳酸镁溶于硝酸中:2H++CO32-=CO2↑+H2O
C.在澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2=CaCO3↓+H2O
D.硫酸氢钠溶液中加入碳酸氢钠溶液:H++HCO3-=CO2↑+H2O
参考答案:A.金属铝溶于盐酸中的离子反应为2Al+6H+=2Al3++3H2↑,故A错误;
B.碳酸镁溶于硝酸中的离子反应为2H++MgCO3=CO2↑+H2O+Mg2+,故B错误;
C.在澄清石灰水中通入过量的CO2的离子反应为OH-+CO2=HCO3-,故C错误;
D.硫酸氢钠溶液中加入碳酸氢钠溶液的离子反应为H++HCO3-=CO2↑+H2O,故D正确;
故选D.
本题解析:
本题难度:简单
3、选择题 ( 4分) 通常条件下PbSO4是一种不溶于水、酸、碱溶液的白色沉淀。但是PbSO4却溶于CH3COONH4溶液得无色溶液(1)。在(1)溶液中再通入H2S气体形成黑色沉淀(2)。结合中学化学有关离子反应发生的条件、离子反应方程式书写规则,写出(1)(2)两种产物形成的离子方程式:
(1)??;
(2)?。
参考答案:(4分)(1) PbSO4 +2 CH3COO- = Pb(CH3COO)2 + SO42-
(2) Pb(CH3COO)2 + H2S =" PbS↓+" 2CH3COOH
本题解析:(1) PbSO4 +2 CH3COO-=Pb(CH3COO)2+SO42-
(2) Pb(CH3COO)2+H2S=PbS↓+2CH3COOH
PbSO4 、PbS是沉淀,写分子形式,Pb(CH3COO)2难电离,写分子形式,H2S、CH3COOH是弱电解质,写分子形式。
本题难度:简单
4、选择题 下列离子方程式正确的是( )
A.铁和盐酸反应:2Fe+6H+=2Fe3++3H2↑
B.氯化铁和铜反应:Fe3++Cu=Fe2++Cu2+
C.将少量CO2通入澄清石灰水:CO2+Ca2++2OH-=CaCO3↓+H2O
D.大理石与盐酸的反应:CO32-+2H+=H2O+CO2↑
参考答案:A.铁和盐酸反应生成Fe2+,反应的离子方程式为Fe+2H+=Fe2++H2↑,故A错误;
B.氯化铁和铜反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,故B错误;
C.将少量CO2通入澄清石灰水生成CaCO3和H2O,反应的离子方程式为CO2+Ca2++2OH-=CaCO3↓+H2O,故C正确;
D.大理石的主要成分为CaCO3,不溶于水,与盐酸反应的离子方程式为CaCO3+2H+=H2O+CO2↑+Ca2+,故D错误.
故选C.
本题解析:
本题难度:一般
5、选择题 下列离子方程式正确的是
A.铁与稀硫酸反应:2Fe + 6H+= 2Fe3++ 3H2↑
B.H2SO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++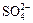 ===BaSO4↓+H2O
===BaSO4↓+H2O
C.氢氧化镁溶于盐酸:Mg(OH)2+2H+=Mg2++2H2O
D.碳酸钙溶于稀盐酸中:CO32-+2H+=H2O+CO2?
参考答案:C
本题解析:略
本题难度:一般