1、选择题 用NA表示阿伏加德罗常数的值,有关下列说法正确的是
A.5.6g铁与稀硝酸反应一定转移0.3NA个电子
B.常温常压下,32g氧气中含有NA个共用电子对
C.常温常压下,11.2L二氧化硫中含有0.5NA个分子
D.在1L?0.1mol/L碳酸钠溶液中CO32-数小于0.1NA
参考答案:D
本题解析:分析:A、铁和硝酸反应可以生成亚铁盐也可以生成铁盐;
B、质量换算物质的量结合氧气分子结构计算共用电子对数
C、依据气体摩尔体积的体积应用分析判断;
D、水溶液中醋酸根离子水解;
解答:A、铁和硝酸反应可以生成亚铁盐也可以生成铁盐,5.6g铁物质的量为0.1mol,生成三价铁盐转移0.3NA个电子,生成二价铁盐转移0.2mol电子;故A错误;
B、32g氧气物质的量为1mol,分子中中含有2NA个共用电子对,故B错误;
C、常温常压下,11.2L二氧化硫物质的量不是0.5mol,故C错误;
D、碳酸根离子水解,1L?0.1mol/L碳酸钠溶液中CO32-数小于0.1NA,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常的应用,主要考查氧化还原反应的产物判断,质量换算物质的量计算微粒数,气体摩尔体积的体积应用,盐类水解的应用,题目难度中等.
本题难度:简单
2、选择题 下图分别是A、B两种物质的核磁共振氢谱,已知A、B两种物 质都是烃类,都含有6个氢原子,试根据两种物质的核磁共振 氢谱推测A、B有可能是下面的
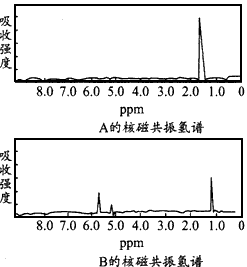
[? ]
A. C3H6,C6H6
B. C2 H6, C3H6
C. C2H6, C6H6
D. C3H6,C2H6
参考答案:B
本题解析:
本题难度:一般
3、填空题 A和B两种有机物可以互溶,有关性质如下
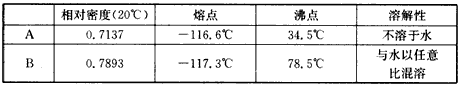
(1)要除去A和B的混合物中的少量A,可采用________方法即可得到B。
A.蒸馏 B.重结晶 C.萃取 D.加水充分振荡,分液
(2)若B的分子式为C2H6O,核磁共振氢谱表明其分子中有三种化学环境不同的氢原子,强度之比为3:2:1。则B的结构简式为__________________。
(3)若质谱图显示A的相对分子质量为74,红外光谱如图所示,则A的结构简式为____________。
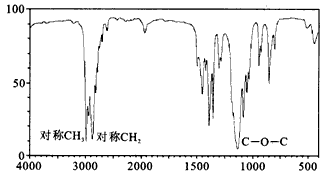
(4)准确称取一定质量的A和B的混合物,在足量氧气中充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增重14.4g和26.4g。计算混合物中A和B的物质的量之比。
参考答案:(1)A
(2)CH3CH2OH
(3)CH3CH2OCH2CH3
(4)1:1
本题解析:
本题难度:一般
4、选择题 已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是?
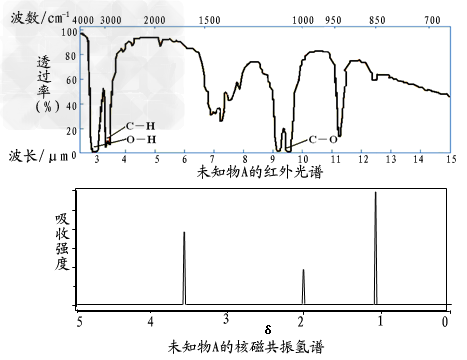
[? ]
A.由红外光谱可知,该有机物中至少含有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子且个数比为1:2:3
C.仅由其核磁共振氢谱可知其分子中的氢原子总数
D.若A的化学式为C2H6O,则其结构简式为CH3CH2OH?
参考答案:C
本题解析:
本题难度:一般
5、选择题 设阿伏加德罗常数为NA,下列说法正确的是
A.标准状况下,11.2L以任意比混合的氮气和氧气所含的原子数为NA
B.一定条件下,0.1mol铝与一定量NaOH溶液充分反应后生成0.1molH2,则转移的电子数约为0.3?NA
C.常温常压下,1mol氦气含有的核外电子数为4NA
D.标状况下,NA个NO分子和0.5NA个O2分子混合后气体的总体积为33.6L
参考答案:A
本题解析:分析:A、根据n=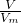 计算混合气体的物质的量,根据N=nNA计算分子数目,二者都是双原子分子,原子数目是分子数目的2倍;
计算混合气体的物质的量,根据N=nNA计算分子数目,二者都是双原子分子,原子数目是分子数目的2倍;
B、反应中H元素的化合价由+1价降低为0价,据此根据氢气的物质的量计算转移电子的物质的量,再根据N=nNA计算转移电子数目;
C、氦气是单原子分子,每个氦气分子含有2个电子;
D、NO与氧气不能共存,反应生成二氧化氮,二氧化氮和四氧化二氮存在化学平衡,据此分析判断.
解答:A、标准状况下,11.2L以任意比混合的氮气和氧气的物质的量为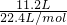 =0.5mol,分子数目为0.5NA,二者都是双原子分子,原子数目是分子数目的2倍为NA,故A正确;
=0.5mol,分子数目为0.5NA,二者都是双原子分子,原子数目是分子数目的2倍为NA,故A正确;
B、反应中H元素的化合价由+1价降低为0价,故生成0.1molH2,则转移的电子数为0.1mol×2×NAmol-1=0.2NA,故B错误;
C、氦气是单原子分子,每个氦气分子含有2个电子,故1mol氦气含有的核外电子数为2NA,故C错误;
D、标准状况下,NA个NO分子为1mol,0.5NA个O2分子为0.5mol,混合后反应2NO+O2=2NO2,生成二氧化氮为1mol,二氧化氮和四氧化二氮存在化学平衡2NO2?N2O4,反应后的气体的物质的量小于中分子总数小于1mol,故标准状况下体积小于22.4L,故D错误;
故选A.
点评:考查常用化学计量的有关计算等,难度中等,选项D为易错点,注意二氧化氮和四氧化二氮存在化学平衡.
本题难度:简单