1、填空题 (1)当K断开时,________上有气泡产生,生成气体对应的离子方程式为__________。
(2)当K闭合时,________片上有气泡。生成气体对应的离子方程式为____________。
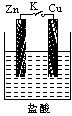
参考答案:(1)Zn;Zn+2H+ = Zn2++H2↑;
(2)Cu;2H++2e- = H2↑
本题解析:
本题难度:一般
2、选择题 某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )
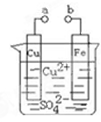
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
参考答案:D
本题解析:A、a和b不连接时,铁片和硫酸铜溶液之间发生置换反应,铁片上会有金属铜析出,正确;B、a和b用导线连接时,形成了原电池,铜作正极,发生的反应为:Cu2++2e-=Cu,正确;C、a和b不连接时,铁片和硫酸铜溶液之间直接发生置换反应, a和b用导线连接时,形成了原电池,加快了铁将金属铜从其盐中置换出来的速度,无论a和b是否连接,铁片均会溶解,溶液从硫酸铜的蓝色逐渐变成硫酸亚铁的浅绿色,正确;D、a和b分别连接直流电源正、负极,构成电解池,阳离子移向阴极铁,所以Cu2+向铁电极移动,错误。
本题难度:一般
3、填空题 (16分)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g)?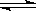 ?CH3OH(g)?ΔH< 0。
?CH3OH(g)?ΔH< 0。
(1)上述反应的平衡常数表达式为K=?,以下有关说法正确的是________
a.恒温、恒容条件下,容器内的压强不发生变化则可逆反应达到平衡
b.一定条件下,H2的消耗速率是CO的消耗速率的2倍时可逆反应达到平衡
c.保持容器体积不变,升高温度可提高CO的转化率
d.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
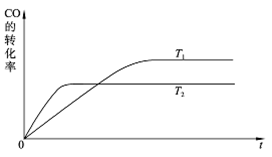
(2)其它条件相同时,在T1、T2(T1< T2)两个不同温度下可逆反应达到平衡,请画出CO的转化率随时间变化的示意图。

(3)已知在常温常压下:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)?ΔH= -a kJ・mol-1
② 2CO(g)+O2(g)=2CO2(g)?ΔH= -b kJ・mol-1
③ H2O(g)= H2O(l)?ΔH= -c kJ・mol-1
则 CH3OH(l)+ O2(g) = CO(g) + 2H2O(l)?ΔH=______________kJ・mol-1。
(4)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如图所示。
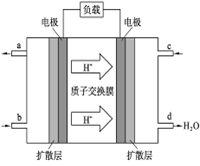
C极发生的电极反应式为:___________________________,工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有______NA个电子发生转移。
(H:1? C:12? O:16)
参考答案:(16分)
(1)c(CH3OH) / c(CO)c2(H2)? (2分) ,A(3分)?
(2)(4分)
(3)(b-a-4c)/ 2(2分)
(4)O2+4e-+4H+ = 2H2O(3分),1.2(2分)
本题解析:(1)a:该可逆反应:正反应气体系数不同,则容器内压强是个变量,何时恒定了,则说明达到平衡。
b:只给出了两个正反应速率,并不能说明正逆反应速率相等,错;
c:正反应是放热反应,升温平衡逆向移动,CO的转化率降低
d:催化剂可改变反应速率但不能改变平衡状态和物质的转化率
(2)该可逆反应,正反应是放热反应,升温,反应速率加快,达到平衡所用时间短;平衡逆向移动,CO的转化率降低
(3)由盖斯定律可得总反应:(①-②+4×③)/2
(4)氢离子向正极移动,氧气在反应中得到电子,因此在正极通入的是氧气,所以电极反应式为O2+4e-+4H+=2H2O。
电池总反应为:2CH3OH+3O2=2CO2+4H2O;反应中电子转移为12e-,故当6.4 g甲醇完全反应时有1.2NA个电子发生转移
本题难度:一般
4、选择题 在一密闭容器中,发生反应:A(g)+B(g)  C(g)+D(g),其化学平衡常数K随温度变化的关系如下表所示,则下列有关判断正确的是
C(g)+D(g),其化学平衡常数K随温度变化的关系如下表所示,则下列有关判断正确的是
T/℃
| 800
| 850
| 1 000
| 1 200
|
K
| 0.9
| 1.0
| 1.7
| 2.4
|
A.若A的浓度增加到原平衡的2倍,则平衡一定正向移动
B.该反应的ΔH>0
C.在850℃条件下,反应达到平衡时,容器中各物质的浓度一定相等
D.A的转化率越大,平衡常数越大
参考答案:B
本题解析:所给反应为两边气体系数相等的可逆反应,升温时K增大,即平衡右移,正反应为吸热反应,也就是说ΔH>0,B正确
A:比如将容器体积减小为原来的一半,各物质的浓度均为原来的两倍,相当于加压,平衡并不移动;
C:在850℃条件下,反应达到平衡时,K=1=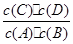 ,而不是各物质的浓度相等。
,而不是各物质的浓度相等。
D:平衡常数只与温度相关,而与A的转化率无必然联系
本题难度:一般
5、选择题 下列叙述中正确的是( )
A.用铂电极电解NaOH溶液,一段时间后,溶液中溶质的质量分数不变
B.用电解法精炼粗铜时,粗铜作阴极
C.用惰性电极电解100mL饱和食盐水,生成112mL氢气(标况)时,氢氧根离子浓度约为0.05mol/L(假定溶液体积仍为100mL)
D.铜锌原电池工作时,正极从外电路得到电子
参考答案:A、用铂电极电解NaOH溶液时,阳极上氢氧根离子失电子生成氧气,阴极上氢离子得电子生成氢气,导致溶液中氢氧化钠的量不变,水的质量减少,所以一段时间后,溶液中溶质的质量分数增大,故A错误;
B、用电解法精炼粗铜时,粗铜作阳极,精铜作阴极,故B错误;
C、用惰性电极电解100mL饱和食盐水,生成112mL氢气(标况)时,阳极上生成112mL氯气,根据电池反应方程式计算生成的氢氧化钠的物质的量.
设生成氢氧化钠的物质的量为x.
2NaCl+2H2O?电解?.?Cl2↑+H2↑+2NaOH
? 22.4L? 2mol
? 0.112L? x
x=0.01mol,氢氧根离子浓度C=nV=0.01mol0.1L=0.1mol/L,故C错误;
D、铜锌原电池工作时,负极上锌失电子发生氧化反应,正极上得电子发生还原反应,电子从负极沿外电路流向正极,所以正极从外电路得到电子,故D正确.
故选D.
本题解析:
本题难度:简单