1、选择题 银锌电池的充电和放电过程可表示为: 2Ag+Zn(OH)2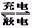 Ag2O+Zn+2H2O,此电池放电时,负极上发生反应的物质是(? )
Ag2O+Zn+2H2O,此电池放电时,负极上发生反应的物质是(? )
A.Ag
B.Zn(OH)2
C.Ag2O
D.Zn
参考答案:D
本题解析:根据原电池工作原理,负极上发生氧化反应.元素化合价会升高,所以在放电过程中被氧化的是Zn,即Zn为负极.
本题难度:一般
2、填空题 (12分)生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式______________。
(2)根据等电子原理,写出CO分子的结构式________。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10―9 。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,若Na2CO3溶液的浓度为2×10―4mo1/L,现将等体积的CaCl2溶液与Na2CO3溶液混合,则生成沉淀所需CaCl2溶液的最小浓度为______mo1/ L。
(4)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是________;甲醛分子的空间构型是_____,中心碳原子的轨道杂化类型为_____。1 mol甲醛分子中σ键的数目为________。
②甲醇可制作燃料电池,以KOH溶液作电解质,向两极分别充入甲醇和空气,工作过程中,负极反应方程式为:___________________。
③已知在常温常压下:
CH3OH(l)+O2(g)= CO(g)+2H2O(g) △H=" -359.8" kJ・mol-1
2CO(g)+O2(g)=2CO2(g) ? △H=" -556.0" kJ・mol-1
H2O(g)=H2O(l)? △H=" -44.0" kJ・mol-1
写出体现甲醇燃烧热的热化学方程式 。
参考答案:(1)1s22s22p63s23p63d104s2
(2)C≡O (3)5.6×10―5
(4)①甲醇分子之间形成氢键,平面三角形,sp2杂化,1.806×1024
②CH3OH-6e-+8OH-=CO32-+6H2O ③CH3OH(l)+3/2O2(g)=CO2(g) +2H2O(l)△H=-725.8kJ/mol
本题解析:(1)Zn的原子序数为30,关键是要注意3d轨道写在4s轨道的前面,电子排布式为1s22s22p63s23p63d104s2或[Ar]3d104s2,(2)依据等电子原理,可知CO与N2为等电子体,N2分子的结构式为:N≡N,互为等电子体分子的结构相似,可写出CO的结构式为C≡O,故答案为:C≡O;
(3)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=1/2×2×10-4mol/L=1×10-4mol/L,根据Ksp=c(CO32-)×c(Ca2+)=2.8×10-9可知,c(Ca2+)=2.8×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L.
(4)①甲醇分子之间形成了分子间氢键,甲醛分子间只是分子间作用力,而没有形成氢键,故甲醇的沸
点高;甲醛为sp2杂化,不含孤电子对,分子的空间构型为平面三角形;1mol甲醛分子中含有2mol碳
氢δ键,1mol碳氧δ键,故含有δ键的物质的量为3mol,数目为1.806×1024个;②正极得到电子,
发生还原反应,同时因为在碱性条件下,则OH-参与反应,根据总方程式可知产物是CO32-和6H2O所以答案为:CH3OH-6e-+8OH-=CO32-+6H2O③根据盖斯定律得 :热方程式1+热化学方程式2×1/2+热化学方程式3×2 则答案为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ/mol
考点:考查共价键类型和热化学方程式书写等相关知识点
本题难度:困难
3、选择题 某种燃料电池是以甲烷(CH4)和空气为原料,以KOH为电解质溶液构成的原电池。电池的总反应类似甲烷在氧气中的燃烧。下列说法正确的是
①每消耗1molCH4可以向外电路提供8mole-
②CH4在负极发生氧化反应,电极反应式是:CH4 + 10OH- - 8e- = CO32- + 7H2O
③燃料电池把化学能直接转化为电能,而不经过热能这一种中间形式,所以它的能量转化效率高,并且减少了对环境的污染
④这种燃料电池要定期更换电解质溶液
A.①②
B.①②③④
C.①③④
D.②④
参考答案:B
本题解析:略
本题难度:简单
4、选择题 锂离子电池已经成为应用最广泛的可充电电池。某种锂离子电池的结构示意图如图,其中两极区间的隔膜只允许Li+通过。电池充电时的总反应化学方程式为:
LiCoO2===Li1-xCoO2+xLi。关于该电池的推论错误的是( )。

A.放电时,Li+主要从负极区通过隔膜移向正极区
B.放电时,负极反应xLi-xe-===xLi+
C.充电时,将电能转化为化学能
D.充电时,负极(C)上锂元素被氧化
参考答案:D
本题解析:A、放电时,化学能转化为电能,相当于原电池装置,阳离子移向正极,正确;B、放电时负极发生氧化反应,Li失去电子成为Li+,正确;C、充电时是把电能转化为化学能,正确;D、充电时,Li元素的化合价由+1价降低为0价,被还原,错误,答案选D。
考点:考查电化学反应原理的应用
本题难度:一般
5、选择题 右图为铅蓄电池的示意图。下列说法正确的是

A.放电时,N为负极,其电极反应式为: PbO2+SO42-+4H++2e-=PbSO4+2H2O
B.放电时,c(H2SO4)不变,两极的质量增加
C.充电时,阳极反应式为:PbSO4+2e-= Pb+SO42-
D.充电时,若N连电源正极,则该极生成PbO2
参考答案:D
本题解析:铅蓄电池中Pb是负极二氧化铅是正极,A不正确;放电时消耗硫酸,所以硫酸的浓度降低,B不正确;充电相当于是放电的逆过程,所以充电时,阳极反应式为PbSO4+2H2O-2e-=PbO2+SO42-+4H+,C不正确,所以正确的答案选D。
点评:该题是基础性试题的考查,难度不大。该题的关键是明确放电和充电的关系,然后结合题干灵活分析即可,该题学生不难得分。
本题难度:简单