1、填空题 (10分)某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
?1?根据下表中数据,在下图中画出X、Y、Z的物质的量n随时间t变化的曲线:
t/min
| X/mol
| Y/mol
| Z/mol
|
0
| 1.00
| 1.00
| 0.00
|
1
| 0.90
| 0.80
| 0.20
|
3
| 0.75
| 0.50
| 0.50
|
5
| 0.65
| 0.30
| 0.70
|
9
| 0.55
| 0.10
| 0.90
|
10
| 0.55
| 0.10
| 0.90
|
14
| 0.55
| 0.10
| 0.90
|
?2?体系中发生反应的化学方程式是_____________;
?3?列式计算该反应在0~3 min时间内产物Z的平均反应速率:______________________;
?4?该反应达到平衡时反应物X的转化率α等于________;
?5?如果该反应是放热反应。在该反应达到上述平衡状态时改变实验条件?温度、压强、催化剂?得到Z的物质的量(mol)随时间t(min)变化的曲线1、2、3?如上右图所示?则曲线1、2、3所对应的实验条件改变分别是:1______________,2______________,3______________。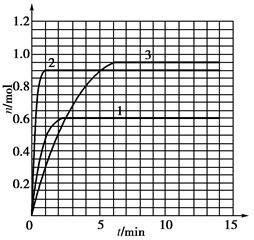
参考答案:?
(1)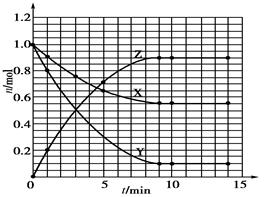 ?(2)?X+2Y
?(2)?X+2Y 2Z?
2Z?
?(3)?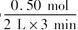 =0.083 mol・L-1・min-1?(4)?45%? ?(5)?升高温度 加入催化剂 增大压强
=0.083 mol・L-1・min-1?(4)?45%? ?(5)?升高温度 加入催化剂 增大压强
本题解析: (1)根据题目中表格给出的数据,在坐标系中找出相应的点,然后用光滑的曲线描点即可。
(1)根据题目中表格给出的数据,在坐标系中找出相应的点,然后用光滑的曲线描点即可。
 (2)根据题意,可以利用“三步法”求解
(2)根据题意,可以利用“三步法”求解
 ? aX? +? bY
? aX? +? bY cZ
cZ
 开始? 1.00? 1.00? 0
开始? 1.00? 1.00? 0
 转化? 0.45? 0.9? 0.9
转化? 0.45? 0.9? 0.9
 平衡? 0.55? 0.1? 0.9
平衡? 0.55? 0.1? 0.9
 根据各物质的量之比可得体系中发生反应的化学方程式是: X+2Y
根据各物质的量之比可得体系中发生反应的化学方程式是: X+2Y 2Z。
2Z。
 (3)根据图像可知在3min时,生成物Z的物质的量为0.5mol,其平均速率为
(3)根据图像可知在3min时,生成物Z的物质的量为0.5mol,其平均速率为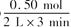 =0.083mol/L・min。
=0.083mol/L・min。
 (4)X的转化率等于
(4)X的转化率等于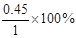 =0.45。
=0.45。
 (5)由题目所给图象可知,在1中,平衡时Z的物质的量小于原平衡的物质的量,说明平衡逆向移动,条件为升高温度。在2中,平衡时Z的物质的量与原平衡相同,且速率加快,条件为加入催化剂;在3中,平衡正向移动,且速率加快,条件为加压。
(5)由题目所给图象可知,在1中,平衡时Z的物质的量小于原平衡的物质的量,说明平衡逆向移动,条件为升高温度。在2中,平衡时Z的物质的量与原平衡相同,且速率加快,条件为加入催化剂;在3中,平衡正向移动,且速率加快,条件为加压。
点评:本题考查化学反应速率和化学平衡的综合运用,注意图像和有关计算。
本题难度:困难
2、选择题 在20℃,5.05×105Pa条件下,密闭容器中进行反应2A(g)+xB(g) 4C(g),达平衡时c(A)=1.00mol?L-1,现将压强减小到1.01×105Pa,建立平衡后,c(A)=0.18mol?L-1,则下列说法正确的是?(? )
4C(g),达平衡时c(A)=1.00mol?L-1,现将压强减小到1.01×105Pa,建立平衡后,c(A)=0.18mol?L-1,则下列说法正确的是?(? )
A.系数x >2
B.若增大该体系的压强,平衡向左移动,化学平衡常数变小
C.若增大该体系的压强,平衡向右移动,化学平衡常数不变
D.该反应的化学平衡常数表达式是K=
参考答案:D
本题解析:A.在5.05×105Pa条件下达平衡时c(A)=1.00mol?L-1,现将压强减小到1.01×105Pa,压强为原来是五分之一,若平衡不发生移动,则建立平衡后,A的浓度也应该为原来的五分之一,即c(A)=0.200mol/L.但是却是c(A)=0.18mol?L-1。说明减小压强,平衡正向移动。根据平衡移动原理,减小压强,平衡向气体体积增大的方向移动。所以2+x<4.所以x=1.错误。B.若增大该体系的压强,平衡向气体体积减小的方向,即向左移动。但是化学平衡常数只与温度有关。温度不变,化学平衡常数也不变。错误。C.若增大该体系的压强,平衡向气体体积减小的方向,即向左移动,由于温度不变,所以化学平衡常数不变。错误。D.化学平衡常数是可逆反应达到平衡状态时各生成物 幂指数的乘积与各反应物浓度幂指数乘积的比,对该反应来说,其化学平衡常数表达式是K= 。正确。
。正确。
本题难度:一般
3、选择题 已知NO2和N2O4可以相互转化:2NO2(g)  N2O4(g)? ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是
N2O4(g)? ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是
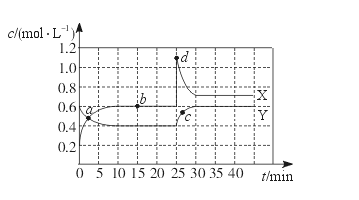
A.如混合气体的压强不变,说明反应已达化学平衡状态
B.a、b、c、d四个点中,表示化学反应处于平衡状态的点是b点
C.25~30 min内用NO2表示的平均化学反应速率是0.08 mol・L-1・min-1
D.反应进行至25 min时,曲线发生变化的原因是增加N2O4浓度
参考答案:D
本题解析:反应是体积减小的,所以当压强不再发生变化时,可以说明反应已经达到平衡状态,A正确。根据图像可知,只与b点物质点浓度不再发生变化,所以b点是平衡状态,B正确。25~30 min内用NO2的浓度变化量是1.1mol/L-0.7mol/L=0.4mol/L,所以NO2的反应速率是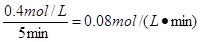 ,C正确。反应进行至25 min时,物质的浓度都是增大的,因此应该是增大压强,平衡向正反应方向移动,D不正确,答案选D。
,C正确。反应进行至25 min时,物质的浓度都是增大的,因此应该是增大压强,平衡向正反应方向移动,D不正确,答案选D。
本题难度:一般
4、选择题 已知H2(g)+I2(g) 2HI(g), 现有相同容积的体积可变的两个绝热容器甲和乙,甲中加入H2和I2各0.1mol ,乙中加入HI 0.2mol,起始温度相同的条件下分别达到平衡。下列说法正确的是
2HI(g), 现有相同容积的体积可变的两个绝热容器甲和乙,甲中加入H2和I2各0.1mol ,乙中加入HI 0.2mol,起始温度相同的条件下分别达到平衡。下列说法正确的是
A.平衡时甲、乙两容器体积相等
B.平衡时甲、乙两容器中c(H2)相等
C.平衡时甲、乙两容器中反应速率v(H2)相等
D.平衡时甲、乙两容器中气体总的物质的量相等
参考答案:D
本题解析:由于反应的容器是绝热的,而正反应与逆反应的热效应是相反的,即甲、乙两个容器中平衡时的温度不同,因此平衡状态是不同的。但根据反应的方程式可知,反应前后气体的物质的量是相同的,所以选项D正确,其余选项都是错误的,答案选D。
本题难度:一般
5、选择题 温度体积固定的容器中建立2NO2 N2O4平衡,平衡时NO2与N2O4物质的量浓度之比为Φ,条件不变的情
N2O4平衡,平衡时NO2与N2O4物质的量浓度之比为Φ,条件不变的情 况下,分别再充入NO2和再充入N2O4,平衡后会引起Φ的变化正确的是:
况下,分别再充入NO2和再充入N2O4,平衡后会引起Φ的变化正确的是:
A.都引起Φ增大
B.充入NO2引起Φ增大,充入N2O4引起Φ减小
C.都引起Φ减小
D.充入NO2引起Φ减小,充入N2O4引起Φ增大
参考答案:C
本题解析:略
本题难度:一般