1、选择题 下列说法正确的是( )
A.铅蓄电池放电时铅电极发生还原反应
B.电解饱和食盐水在阳极得到氯气,阴极得到金属钠
C.给铁钉镀铜可采用CuSO4作电镀液
D.生铁浸泡在食盐水中发生析氢腐蚀
参考答案:A.铅蓄电池放电时铅电极为原电池的负极,发生氧化反应,正极发生还原反应,故A错误;
B.电解饱和食盐水得到氢气、氯气和氢氧化钠,阴极上得到氢气和氢氧化钠,故B错误;
C.电镀时用含镀层金属的阳离子的盐做电解质溶液,则给铁钉镀铜可采用CuSO4作电镀液,故C正确;
D.生铁浸泡在食盐水中发生吸氧腐蚀,在酸性溶液中发生析氢腐蚀,故D错误.
故选C.
本题解析:
本题难度:一般
2、填空题 天然气、煤炭气(CO、H2)的研究在世界上相当普遍。其中天然气和二氧化碳可合成二甲醚,二甲醚与水蒸气制氢气作为燃料电池的氢能源,比其他制氢技术更有优势。主要反应为:
①CH3OCH3(g) +H2O(g) 2CH3OH(g)?△H= 37Kj・mol-1
2CH3OH(g)?△H= 37Kj・mol-1
②CH3OH(g)+H2O(g)  3 H2(g)+CO2(g)?△H =49Kj・mol-1
3 H2(g)+CO2(g)?△H =49Kj・mol-1
③CO2(g) +H2(g)  CO(g) +H2O(g)?△H=41.3Kj・mol-1
CO(g) +H2O(g)?△H=41.3Kj・mol-1
其中反应③是主要的副反应,产生的CO对燃料电池Pt电极有不利影响。
请回答下列问题:
(1)二甲醚可以通过天然气和CO2合成制得,该反应的化学方程式为?。
(2)CH3OCH3(g)与水蒸气制氢气的热化学方程式为 ?。
(3)下列采取的措施和解释正确的是?。(填字母序号)
A.反应过程在低温进行,可减少CO的产生
B.增加进水量,有利于二甲醚的转化,并减少CO的产生
C.选择在高温具有较高活性的催化剂,有助于提高反应②CH3OH的转化率
D.体系压强升高,虽然对制取氢气不利,但能减少CO的产生
(4)煤炭气在一定条件下可合成燃料电池的另一种重要原料甲醇,反应的化学方程式为:
CO (g) +2H2(g)  CH3OH(g)?△H <0。现将l0mol CO与20mol H2置于密闭容器中,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(
CH3OH(g)?△H <0。现将l0mol CO与20mol H2置于密闭容器中,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(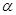 )与温度、压强的关系如下图所示。
)与温度、压强的关系如下图所示。
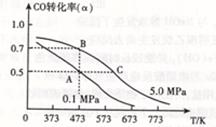
①自反应开始到达平衡状态所需的时间tA?tB(填“大于”、“小于”或“等于”)。
②A、C两点的平衡常数KA?KC(填“大于”、“小于”或“等于”)。
(5)某工作温度为650oC的熔融盐燃料电池,是以镍合金为电极材料,负极通人煤炭气(CO、H2),正极通人空气与CO2的混合气体,用一定比例的Li2CO3和Na2CO3混合物做电解质。请写出正极的电极反应式?____?。
参考答案:(1)3CH4+CO2→2CH3OCH3?
(2)CH3OCH3(g) +3H2O(g)  6H2(g)+2CO2(g)?△H= 135kJ・mol-1
6H2(g)+2CO2(g)?△H= 135kJ・mol-1
(3) ABD?(4)①大于?②大于?(5)O2+4e-+2CO2= 2CO32-
本题解析:本题是有关化学反应原理的综合题。(1)根据原子守恒书写方程式;(2)给出的三个方程式中第③是副反应,所以CH3OCH3(g)与水蒸气制氢气的热化学方程式应是①+2②得到,△H也这样计算。
CH3OCH3(g) +3H2O(g) 6H2(g)+2CO2(g)?△H= 135kJ・mol-1
6H2(g)+2CO2(g)?△H= 135kJ・mol-1
(3)A、反应③是吸热反应,降低温度平衡逆向移动,减少CO的产生,正确;B、对反应①、②来说,水是反应物,增加进水量,促进二甲醚的转化;对于反应③,水是生成物,增加水的量会抑制该反应正向进行,减少CO的产生,正确;C、催化剂不能改变反应物的转化率,只能改变反应速率,错误;D、增大压强对于反应②逆向移动,制取的氢气量减少,但对于反应③,增大压强水的浓度增大,使平衡逆向移动,减少CO的产生,正确。(4)B点压强大,反应速率快,先达到平衡,用时少;K只和温度有关,温度高,该反应逆向移动,K值大,所以KA大于KC;书写电极反应式时要确定正极反应物和产物,要明确介质,确定氧的存在微粒。
本题难度:困难
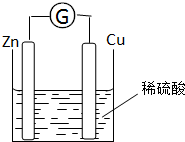
3、简答题 将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图:
(1)锌片上发生的电极反应:______;铜片上发生的电极反应:______;
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为47g,试计算产生标准状况氢气的体积为多少L?(请写出计算过程)______.
参考答案:1)该原电池中,锌易失电子发生氧化反应而作负极,电极反应式为:Zn-2e-=Zn2+,铜作正极,正极上氢离子得电子发生还原反应,电极反应式为:2H++2e-=H2↑,
故答案为:Zn-2e-=Zn2+;2H++2e-=H2↑;
(2)负极上锌生成锌离子进入溶液而导致质量减少,正极上氢离子得电子生成氢气,所以正极质量不变,两个电极减少的质量是锌的质量,锌和稀硫酸反应离子方程式为2H++Zn=Zn2++H2↑,
根据锌和氢气之间的关系式得氢气的体积=(60g-47g)65g/mol1×1×22.4L/mol=4.48L,
故答案为:4.48L.
本题解析:
本题难度:简单
4、选择题 某原电池的电池反应为Fe+2Fe3+→3Fe2+,与此电池反应相符的原电池是
[? ]
A.铜片、铁片、FeCl3溶液组成的原电池
B.石墨、铁片、Fe(NO3)3溶液组成的原电池
C.铁片、锌片、Fe2(SO4)3溶液组成的原电池
D.银片、石墨、Fe(NO3)2溶液组成的原电池
参考答案:AB
本题解析:
本题难度:简单
5、选择题 (2014届上海市六校高三第二次联考化学试卷)
铁棒和石墨棒用导线连接后,浸入0.01mol/L的氯化钠溶液中,可能出现的现象是
A.铁棒附近产生OH-
B.铁棒质量减少
C.石墨棒上放出氢气
D.石墨棒上放出氧气
参考答案:B
本题解析:
铁棒和石墨棒用导线连接后,浸入0.01mol/L的氯化钠溶液形成了原电池,由于活动性Fe>C。所以Fe作负极,发生的电极反应为Fe-2e-=Fe2+。C作正极。因为是中性溶液,所以在正极上发生反应:O2+4e-+2H2O=4OH-。在溶液中2Fe +O2+2H2O=2Fe(OH)2.
4Fe(OH)2+O2+2H2O=4Fe(OH)3.所以Fe会减少。在C棒附近产生OH-。正确选项为B。
本题难度:一般