1、填空题 (14分)
I.甲、乙、丙、丁四种物质存在转化关系:
(1)若甲、乙均为空气主要成分,甲所含元素的简单阴离子的结构示意图为 。
(2)若乙是生活常见金属单质,丙→丁的离子方程式为 。
(3)若丙既能与强酸又能与强碱反应,则丙的化学式为 (任写1种)。
II.一定温度下,容积为1 L的密闭容器中投入0.5 mol PCl5(g),存在平衡:PCl5(g) PCl3(g)+ Cl2(g)。反应过程中测得部分数据如下表:
PCl3(g)+ Cl2(g)。反应过程中测得部分数据如下表:
时间
| n(PCl5)/mol
| n(PCl3)/mol
| n(Cl2)/mol
|
0
| 0.5
| 0
| 0
|
t1
| 0.45
|
|
|
t2
|
| 0.1
|
|
t3
| 0.4
|
|
|
(4)t1时刻,测得反应吸收的热量为a kJ。PCl3(g)与Cl2(g)反应的热化学反应方程式为 。
(5)t2时:v正来源:www.91exam.org v逆(填“>”、“<”或“=”)。
(6)相同温度下,改为往容器中投入0.2 mol PCl5(g)、0.2 mol PCl3(g)、0.1 mol Cl2(g),到达平
衡前,PCl5的物质的量将 (填“增大”、“减小”、“不变”)。
2、填空题 (10分)2SO2(g) + O2(g) = 2SO3 (g)反应过程的能量变化如图所示。已知1mol SO2 (g)氧化为1mol SO3(g)的 ΔH= ―99kJ・mol-1。请回答下列问题:
ΔH= ―99kJ・mol-1。请回答下列问题:
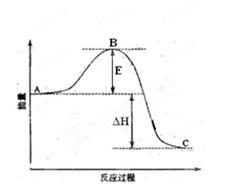
 (1)图中A、C分别表示 ,E的大小对该反应的反应热
(1)图中A、C分别表示 ,E的大小对该反应的反应热
(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”或“降低”),△H (填“变大”、“变小”或“不变”),
 (2)图中△H= KJ・mol-1;
(2)图中△H= KJ・mol-1;
3、选择题 图中的曲线是表示其他条件一定时,2NO+O2 2NO2
2NO2
4、简答题 将CoCl2溶于浓盐酸中能形成CoCl42-.溶液中存在如下平衡:CoCl42-(蓝色)+6H2O?Co(H2O)62+(粉红色)+4Cl-.
(1)一般情况下,CoCl2溶液呈紫色,将盛有CoCl2溶液的试管放在热水中溶液逐渐变成蓝色,则正反应方向为______反应(填“吸热”或“放热”).
(2)该反应平衡常数表达式为______,加水稀释平衡向______方向(填“正”或“逆”)移动.
(3)向溶液中加入少量AgNO3固体,溶液颜色变为______色.
5、选择题 将等物质的量的X气体和Y气体在一绝热恒容的容器中混合,并在一定条件下使反应 X(g)+Y(g)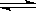 Z(g)达到平衡,正反应速率随时间的变化如图所示,下列叙述不正确的是(?)
Z(g)达到平衡,正反应速率随时间的变化如图所示,下列叙述不正确的是(?)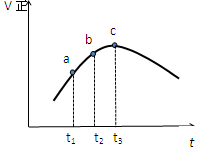
A.X的浓度大小:a>b>c
B.混合气体的平均相对分子质量t1时比t2时小
C.在c点时反应达到平衡
D.反应物的总能量高于生成物的总能量