1、选择题 下列装置中,都伴随有能量变化,其中是由化学能转变为电能的是
[? ]
A. 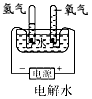
B. 
C. 
D. 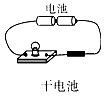
参考答案:D
本题解析:
本题难度:简单
2、选择题 化学反应一般均会伴随着能量变化,对CH4在O2中燃烧的反应,正确的是
A.该反应为吸热反应
B.该反应为放热反应
C.断裂C-H键吸收能量
D.生成H-O键吸收能量
参考答案:BC
本 题解析:甲烷燃烧是放热反应,A不正确,B正确。断键是吸热的,形成化学键是放热的,C正确,D不正确,答案选BC。
点评:该题是中等难度的试题,试题基础性强,侧重对学生基础知识的巩固与训练。有利于培养学生灵活运用基础知识解决实际问题的能力,提高学生的应试能力。该题的关键是明确反应热的含义和计算依据,并能结合题意灵活运用即可。
本题难度:简单
3、填空题 (5分)依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_________________________________________。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g)="=" 2Fe(s)+3CO2(g)?△H=- A kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g)?△H=- B kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g)?△H= + C kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式:
? ?
?
参考答案:(共5分)
(1)CH3OH(l)+3/2? O2(g)=CO2(g) +2H2O(l) △H="-725.76kJ/mol?" (2分)
△H="-725.76kJ/mol?" (2分)
(2) CO (g)+ FeO (s)=CO2(g) +Fe (s)?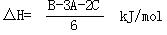 ?(3分)
?(3分)
本题解析:略
本题难度:一般
4、选择题 某反应能量变化如右下图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列叙述正确的是

A.该反应为放热反应
B.催化剂能改变反应的焓变
C.催化剂能降低反应的活化能
D.逆反应的活化能大于正反应的活化能
参考答案:C
本题解析:A、总能量:反应物<生成物,则该反应是吸热反应,错误;B、催化剂只能降低反应的活化能,不能改变反应的焓变,错误;D、读图可知活化能:正反应>逆反应,错误。
本题难度:简单
5、选择题 下列反应中生成物的总能量大于反应物的总能量的是(?)
A.铝粉与氧化铁的反应
B.氯化铵与Ba(OH)2・8H2O反应
C.锌片与稀硫酸反应
D.钠与冷水反应
参考答案:B
本题解析:生成物的总能量大于反应物的总能量的是吸热反应,铝粉与氧化铁的反应是铝热反应。锌片与稀硫酸反应、钠与冷水反应都是放热反应。氯化铵与Ba(OH)2・8H2O反应
是吸热反应。
本题难度:简单