1、选择题 已知可发生反应:2Fe2+ +Br2 ==2Fe3+ +2Br-,2Fe3++2I- ==2Fe2+ +I2。向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。则下列有关说法中正确的是
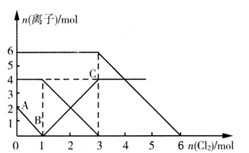
[? ]
A.还原性:Fe2+ >I-> Br-
B.当通入2 mol Cl2时,溶液中发生的离子反应可表示为2Fe2++2I-+2Cl2==2Fe3++I2+4Cl-
C.原混合溶液中FeBr2的物质的量为6 mol
D.原溶液中n(Fe2+):n(I-):n(Br-)=1:1:3
参考答案:B
本题解析:
本题难度:一般
2、选择题 下列说法正确的是( )
A.向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中
减少
B.25℃时,pH=2的一元酸溶液与pH=12的一元碱溶液等体积混合,所得溶液pH一定等于7
C.在(NH4)2Fe(SO4)2溶液中,c(SO)>c(NH)>c(Fe2+)>c(H+)>c(OH-)
D.pH相同的NaOH和氨水两种稀溶液,若稀释后pH仍相同,则稀释的倍数相同
参考答案:A.由于(NH4)2SO4=2NH4++SO42-,溶液中NH4+浓度增大,抑制氨水的电离,则溶液中C(OH-)C(NH3?H2O)减少,故A正确;
B.如酸为弱电解质,则反应后溶液呈酸性,如为强电解质,则反应后呈中性,故B错误;
C.溶液呈酸性,其中c(SO42-)最大,NH4+和Fe2+水解都呈酸性,相互抑制,水解程度较小,则有c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-),故C正确;
D.氨水为弱电解质,加水促进电离,pH相同的NaOH和氨水两种稀溶液,若稀释后pH仍相同,氨水稀释体积较大,故D错误.
故选AC.
本题解析:
本题难度:一般
3、选择题 下列溶液中离子浓度的关系一定正确的是
[? ]
A.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液:c(CH3COO-)>c(CO32-)>c(C6H5-)
B.pH=3的一元酸HX溶液和pH=11的一元碱MOH溶液等体积混合:c(M+)=c(X-)>c(H+)=c(OH-)
C.等物质的量的二元弱酸H2X与其钾盐K2X的混合溶液中:c(K+)=c(H2X)+c(HX-)+c(X2-)
D.氨水中逐滴加入盐酸得到的酸性溶液:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
参考答案:C
本题解析:
本题难度:一般
4、选择题 常温时,以下4种溶液pH最大的是
[? ]
A.0.01mol・L-1氨水溶液
B.0.02mol・L-1氨水与0.02mol・L-1盐酸溶液等体积混合液
C.0.03mol・L-1氨水与0.01mol・L-1盐酸溶液等体积混合液
D.pH =2的盐酸与pH =12的Ba(OH)2溶液等体积混合液
参考答案:A
本题解析:
本题难度:一般
5、选择题 100mL?0.1mol/L的盐酸与50mL?0.2mol/L的氨水混合,充分反应后,所得溶液中各种离子浓度关系正确的是( )
A.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.c(Cl-)=c(NH4+)>c(OH-)=c(H+)
C.c(H+)+c(NH4+)=c(Cl-)+c(OH-)
D.c(H+)+c(Cl-)=c(NH4+)+c(NH3?H2O)+c(OH-)
参考答案:C
本题解析:
本题难度:简单