1��ѡ���� ����ɫ����Һ�У����ܴ���������������ǣ�������
A��K+��Ba2+��SO42-��NO3-
B��K+��Na+��HCO3-��NO3-
C��OH-��HCO3-��Ca2+��Na+
D��Ba2+��Na+��OH-��NO3-
�ο��𰸣�A����Ba2+��SO42-�ܽ�����ɳ��������ܹ��棬�����Ӿ�Ϊ��ɫ����Aѡ��
B�����������֮�䲻��Ӧ�����ܹ��棬��B��ѡ��
C����OH-��HCO3-��Ca2+�ܽ������ˮ�ͳ��������ܹ��棬�����Ӿ�Ϊ��ɫ����Cѡ��
D�����������֮�䲻��Ӧ�����ܹ��棬��D��ѡ��
��ѡAC��
���������
�����Ѷȣ���
2��ѡ���� �����£����и���������ָ����Һ��һ���ܴ����������?
[? ]
A��������ˮ�У�Cl����NO3����Na+?��SO32��
B��c(H+)=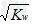 ����Һ�У�K+��Fe3+?��Cl����SO42��
����Һ�У�K+��Fe3+?��Cl����SO42��
C������������Һ�У�Cu2+��NH4+��NO3-��ClO4-?
D��ʹ��ɫʯ����ֽ��������Һ�У�CH3COO����HCO3����Na+��K+
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� ��������Һ�У��ܴ��������һ��������
A��pH��1����Һ�У�NH4+��Fe2+��SO42-��Cl��
B��ͨ�����SO2�������Һ�У�Fe3+��NO3����Ba2+��H+
C��c(Al3+)��0.1 mol/L����Һ�У�Na+��K+��AlO2����SO42-
D����ˮ�������c(H+)��1��10��13mol/L����Һ�У�Na+��HCO3����Cl����Br��
�ο��𰸣�A
���������A����ȷ��B������ȷ��Fe3+��NO3����H�� ���HNO3���ܱ�SO2��ԭ��C������ȷ��Al3����3AlO2�D��6H2O="4Al" (OH)3��;?D������ȷ����ˮ�������c(H+)��1��10��13mol/L����Һ���������Ի���ԣ�HCO3�D�����ܹ��档ѡA��
�����Ѷȣ�һ��
4��ѡ���� ��ij����Na2CO3��NaAlO2����Һ����μ���1 mol��L�����ᣬ�����Һ��CO32-��HCO3-��AlO2-��Al3+�����ʵ���(n)�������������(V)�ı仯��ϵ����ͼ��ʾ������˵������ȷ����
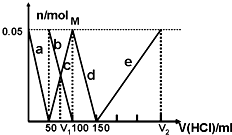
A��a���߱�ʾ������Һ��A1O2-���ʵ�����������������ı仯��ϵ
B������Һ��Na2CO3��NaAlO2���ʵ������
C��M�㴦����HCO3-���ʵ���Ϊ0.05 mol
D��V1��V2��1��5
�ο��𰸣�D
���������Na2CO3��NaAlO2�Ļ����Һ����μ���1mol?L-1�����ᣬ���ȣ�������ӦAlO2-+H++H2O�TAl��OH��3����a�߱�ʾAlO2-����ͼ��֪AlO2-��Ӧ��ϣ���������50mL�����ݷ���ʽ��֪n��AlO2-����n��H+����0.05mol��1mol/L��0.05mol���ڶ��Σ�AlO2-��Ӧ��ϣ�������ӦCO32-+H+�THCO3-��b�߱�ʾCO32-��c�߱�ʾHCO3-����ͼ��֪CO32-��Ӧ��ϣ��ýμ�������100mL-50mL��50mL�����ݷ���ʽ��֪n��CO32-����n��H+����0.05mol��1mol/L��0.05mol�������Σ�CO32-��Ӧ��ϣ�������ӦHCO3-+H+�TCO2��+H2O��d�߱�ʾHCO3-����ͼ��֪HCO3-��Ӧ��ϣ��ýμ�������150mL��100mL��50mL�����ݷ���ʽ��֪n��HCO3-����n��H+�������ĽΣ�������ӦAl��OH��3+3H+�TAl3++3H2O��e�߱�ʾAl3+����ͼ��֪Al��OH��3��Ӧ��ϣ����ݷ���ʽ��֪n��H+����3n[Al��OH��3]��3��0.05mol��0.15mol���ýμ����������Ϊ0.15mol��1mol/L��0.15L��150mL����A��������������֪��a���߱�ʾ�����ӷ���ʽΪ��AlO-2+H++H2O��Al��OH��3������A��ȷ��B��������������֪��ԭ�����Һ�е�CO32-��AlO-2�����ʵ���֮��Ϊ0.05mol��0.05mol��1��1����B����C��������������֪M��ʱ��Һ��CO32-��ȫת��ΪHCO3-�����ʵ���Ϊ0.05mol����C��ȷ��D����Һ��n��CO32-����0.05mol��V1ʱ��Һ��̼��������ӵ���̼�������Ϊ0.025ml���ɷ�ӦCO32-+H+��HCO3-��֪����Ҫ����Ϊ0.025mol����������Ϊ0.025mol��1mol/L��0.025L��25mL����V1��50mL+25mL��75mL��������������֪��V2��150mL+150mL��300mL����V1��V2��75mL��300mL��l��4����D����ѡ��D��
�����Ѷȣ�һ��
5��ѡ���� ���и�������һ���ܴ���������� ��������
A���ں��д���AlO2������Һ�У�HCO3����Na+��Cl����K��
B���ڣ�10��12��Һ�У�Na+��K+��CO32����NO3��
C������ʹAl2O3�ܽ����Һ�У�NH4+�� Na+��SO42����Cl��
Na+��SO42����Cl��
D������ʹ���ȱ�����Һ�У�K+��I����Cl����NO3-