1��ѡ���� ��֪��H+(aq)+OH-(aq) ��H2O(l)�� ��H��-57��3 kJ��mol-1���ֽ�һ������ϡ���ᡢŨ���ᡢϡ����ֱ��1L 1mol��L-1��NaOH��Һǡ����ȫ��Ӧ���䷴Ӧ�ȷֱ�Ϊ��H1����H2����H3��,���H1����H2�͡�H3�Ĵ�С��ϵΪ
A����H1����H2
B����H2����H1
C����H3����H2
D����H1����H3
�ο��𰸣�C
���������H+��aq��+OH-��aq���TH2O��l������H=-57��3kJ?mol-1���к�����ǿ��ǿ��ϡ��Һ��ȫ��Ӧ����1molˮ�ų���������һ������ϡ�����1L?1mol?L-1��NaOH��Һǡ����ȫ��Ӧ����57��3kJ��Ũ�����1L?1mol?L-1��NaOH��Һǡ����ȫ��Ӧ���ܽ�����з��ȣ���Ӧ���ȴ���57��3kJ��������������ʴ��ڵ���ƽ�⣬������������ỵ̄������1L?1mol?L-1��NaOH��Һǡ����ȫ��Ӧ����С��57��3kJ����Ӧ�ʱ��Ǹ�ֵ�����ԡ�H3����H1����H2����ѡC��
�����Ѷȣ�һ��
2������� ���ǵ����Ϻ�����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���á���ش��������⣺
��1����ͼ��1 mol NO2��1mol CO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ?��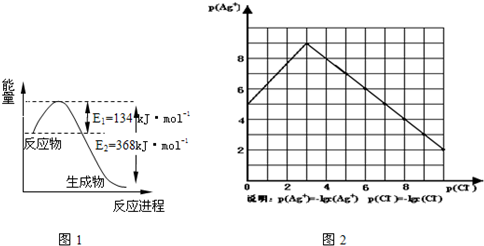
��2����0.5L���ܱ������У�һ�����ĵ����������������»�ѧ��Ӧ��N2(g)+3H2(g)  2NH3(g)��H<0�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���ұ���������������⣻
2NH3(g)��H<0�仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���ұ���������������⣻
?
���ԱȽ�K1��K2�Ĵ�С��K1____K2����д��>������=����<����
�����и�������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������____һ���������ĸ��
a��������N2��H2��NH3��Ũ��֮��Ϊ1��3��2
b��v��N2����=3v��H2����
c��������ѹǿ���ֲ���
d�����������ܶȱ��ֲ���
��400��ʱ����Ӧ2NH3(g)  N2(g)+3H2(g)�Ļ�ѧƽ�ⳣ����ֵΪ?�������NH3��N2��H2�����ʵ����ֱ�Ϊ3mol��2mol��1molʱ����÷�Ӧ��v��N2���� __? v��N2���棨��д��>������=����<��=��
N2(g)+3H2(g)�Ļ�ѧƽ�ⳣ����ֵΪ?�������NH3��N2��H2�����ʵ����ֱ�Ϊ3mol��2mol��1molʱ����÷�Ӧ��v��N2���� __? v��N2���棨��д��>������=����<��=��
�ο��𰸣���1��NO2(g)+CO(g) CO2(g)+NO(g);��H����234kJ/mol?��2�� �� >?��? c?��? 2? >
CO2(g)+NO(g);��H����234kJ/mol?��2�� �� >?��? c?��? 2? >
�����������1����ͼ��֪��NO2��CO��Ӧ���Ȼ�ѧ����ʽΪ��NO2(g)+CO(g) CO2(g)+NO(g);��H����234kJ/mol ����2�� �������¶Ȼ�ѧƽ�������ȷ�Ӧ�����ƶ������ڸ÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����������¶Ȼ�ѧƽ�����淴Ӧ�����ƶ���ƽ��Խ���淴Ӧ�����ƶ�����Ӧ��ƽ�ⳣ����ԽС������K1 >K2����aƽ��ʱ�����ʵ�Ũ������ʼ��������ʵĶ����йء�ֻҪƽ��ʱ�������ʵ�Ũ�Ȳ��䣬��Ӧ�ʹﵽ��ƽ�⡣����b�����κ�ʱ�̶���3v��N2����=v��H2��������v��N2����=3v��H2���棬�����һ��ʽ�ӿɵ�9 v��H2����= v��H2����������V��H2����>V��H2���档��Ӧδ�ﵽƽ�⡣����c�������������ݻ����䣬����Ӧ�ﵽƽ�⣬�������ʵ����ʵ������䣬������ѹǿҲ���ֲ��� ����ȷ��? d����Ӧ���۽��е�ʲô�̶ȣ����������ᷢ���仯����ô�κ�ʱ�̻��������ܶȶ����ֲ��䡣���Բ��ܸ����������ݻ��������жϷ�Ӧ�ﵽƽ�⡣����ѡ��Ϊ��C. ��400��ʱ��2NH3(g)
CO2(g)+NO(g);��H����234kJ/mol ����2�� �������¶Ȼ�ѧƽ�������ȷ�Ӧ�����ƶ������ڸ÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����������¶Ȼ�ѧƽ�����淴Ӧ�����ƶ���ƽ��Խ���淴Ӧ�����ƶ�����Ӧ��ƽ�ⳣ����ԽС������K1 >K2����aƽ��ʱ�����ʵ�Ũ������ʼ��������ʵĶ����йء�ֻҪƽ��ʱ�������ʵ�Ũ�Ȳ��䣬��Ӧ�ʹﵽ��ƽ�⡣����b�����κ�ʱ�̶���3v��N2����=v��H2��������v��N2����=3v��H2���棬�����һ��ʽ�ӿɵ�9 v��H2����= v��H2����������V��H2����>V��H2���档��Ӧδ�ﵽƽ�⡣����c�������������ݻ����䣬����Ӧ�ﵽƽ�⣬�������ʵ����ʵ������䣬������ѹǿҲ���ֲ��� ����ȷ��? d����Ӧ���۽��е�ʲô�̶ȣ����������ᷢ���仯����ô�κ�ʱ�̻��������ܶȶ����ֲ��䡣���Բ��ܸ����������ݻ��������жϷ�Ӧ�ﵽƽ�⡣����ѡ��Ϊ��C. ��400��ʱ��2NH3(g)  N2(g)+3H2(g)�Ļ�ѧƽ�ⳣ���ͷ�ӦN2(g)+3H2(g)
N2(g)+3H2(g)�Ļ�ѧƽ�ⳣ���ͷ�ӦN2(g)+3H2(g)  2NH3(g)�Ļ�ѧƽ�ⳣ����Ϊ��������Ϊ2,������C2(NH3)/C(N2)C3(H2)=62/(4��23)=9/8<2.���Է�Ӧ������Ӧ�����ƶ�����V��N2����> V��N2���档
2NH3(g)�Ļ�ѧƽ�ⳣ����Ϊ��������Ϊ2,������C2(NH3)/C(N2)C3(H2)=62/(4��23)=9/8<2.���Է�Ӧ������Ӧ�����ƶ�����V��N2����> V��N2���档
�����Ѷȣ�һ��
3��ѡ���� ����˵���У�����ȷ����
A����ѧ��Ӧ�м������ʱ仯���������仯
B����ʹû�з�����ѧ�仯��Ҳ�����������ı仯
C���κλ�ѧ��Ӧ�е������仯������Ϊ�����仯
D�����ʵĻ�ѧ�ܿ���ͨ����ͬ�ı仯��ʽת��Ϊ���ܡ����ܵ�
�ο��𰸣�C
�����������ѧ��Ӧ�м������ʱ仯���������仯����A��ȷ����ʹû�з�����ѧ�仯��Ҳ�����������ı仯,����ˮ����������B��ȷ����ѧ��Ӧ�е������仯һ�����Ϊ�����仯��Ҳ�������Ź��ܵȵı仯������C�������ʵĻ�ѧ�ܿ���ͨ����ͬ�ı仯��ʽת��Ϊ���ܡ����ܵȣ���D��ȷ�����Դ�ΪC��
���������⿼���˻�ѧ���������Ǹ߿�������ص㣬���ⲻ�ѡ�
�����Ѷȣ���
4��ѡ���� ����ʵ����ʵ����������Ӧ������ȷ����
ѡ��
| ʵ����ʵ
| ����
|
A
| Na2S2O3��Һ��ϡH2SO4��Һ���ʱ������������ͬ��Na2S2O3��ҺŨ��Խ���������������ʱ��Խ��
| ��������������ʱ������Ӧ��Ũ�Ȼ�ѧ��Ӧ���ʼӿ�
|
B
| �ڻ�ѧ��Ӧǰ�����������ͻ�ѧ���ʶ�û�з����ı�
| ����һ�����μӻ�ѧ��Ӧ
|
C
| ��NH4Cl������Ba(OH)2.8H2O�����Ϻ���ĥ���ձ����¶Ƚ���
| �÷�ӦΪ���ȷ�Ӧ
|
D
| ���ݻ��ɱ���ܱ������з�����Ӧ
H2��g��+ I2��g��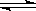 2HI��g���� 2HI��g����
���ݻ���Сһ��
| ����Ӧ���ʼӿ죬�淴Ӧ���ʲ���
�ο��𰸣�AC
���������
��ȷ��AC
A����������������ʱ������Ӧ��Ũ�Ȼ�ѧ��Ӧ���ʼӿ졣
B���ڻ�ѧ��Ӧǰ�����������ͻ�ѧ���ʶ�û�з����ı䣬���������ʸı䣬�������ܲμӷ�Ӧ��
C��NH4Cl������Ba(OH)2.8H2O����Ϊ���ȷ�Ӧ��
D��H2��g��+ I2��g��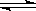 2HI��g�������ݻ���Сһ����Ũ�Ⱦ��������淴Ӧ���ʾ��ӿ죬ֻ�DZ仯�ķ�����ͬ������ƽ�ⲻ�ƶ��� 2HI��g�������ݻ���Сһ����Ũ�Ⱦ��������淴Ӧ���ʾ��ӿ죬ֻ�DZ仯�ķ�����ͬ������ƽ�ⲻ�ƶ���
�����Ѷȣ�һ��
5��ѡ���� ��ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ����ЧӦΪ��H+(aq) +OH-(aq)�TH2O(l)
��H = -57��3kJ/mol���ֱ���1L 0��5mol/L��Ba(OH)2����Һ�м����Ũ����� ϡ�����ϡ���ᣬǡ����ȫ��Ӧ����ЧӦ�ֱ�Ϊ��H1����H2����H3�����й�ϵ��ȷ����
A����H1����H2����H3
B����H1����H2����H3
C����H1����H2����H3
D����H1����H2����H3
�ο��𰸣�A
���������Ũ������ǿ�ҵ���ˮ�ԣ��ܽ���ˮ�ų��������ȣ����ԡ�H1����H�� ϡ���ᡢϡ���ᶼ������������������ӣ�����Һ�з�����ӦH+(aq) +OH-(aq)�TH2O(l)���ų�������H2����H3=��H��������ȷѡ��ΪA��
�����Ѷȣ�һ��
|