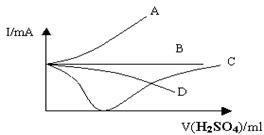
1、选择题 向盛有一定量Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示,主要与溶液中可自由移动的离子浓度有关)近似可用下图中的哪条曲线表示
参考答案:C
本题解析:向氢氧化钡溶液中加入稀硫酸,生成硫酸钡沉淀和水,离子浓度减小,随硫酸的过量,离子浓度又增加,故C项正确。
考点:本题考查电解质溶液导电原因。
本题难度:一般
2、填空题 ①25℃,难溶电解质的溶度积常数:Ksp[CaF2]=1.5×10-10,Ksp[Mg(OH)2]=1.8×10-11,Ksp [Cu(OH)2]=2.2×10-20
②弱电解质在水溶液中存在电离常数:例如一元弱酸HA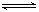 H++A-,其电离常数表达式 Ka= c(H+)・c (A-)/ c (HA)(各浓度为平衡时浓度)。该常数与浓度、压强无关,只是温度的函数。25℃,醋酸的Ka=1.76×10-5
H++A-,其电离常数表达式 Ka= c(H+)・c (A-)/ c (HA)(各浓度为平衡时浓度)。该常数与浓度、压强无关,只是温度的函数。25℃,醋酸的Ka=1.76×10-5
③25℃时,2.0×10-3mol・L-1氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到
c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
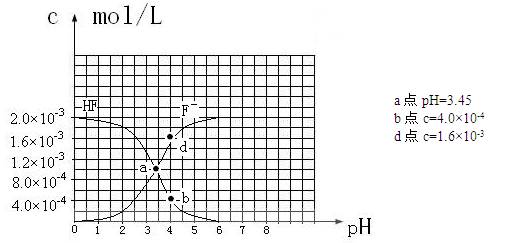
请根据以上信息回答下列问题:
(1)25℃时,向浓度均为0.1 mol・L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为 。
(2)25℃时,HF电离常数的数值Ka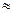 ,列式并说明得出该常数的理由 。
,列式并说明得出该常数的理由 。
(3)25℃时,向浓度均为0.1 mol・L-1的相同体积的HF和醋酸两种溶液中分别加入相同的足量锌粒,初始时产生氢气的速率关系为 (填“>”“=”或“<”,下同)。反应结束后,产生氢气的物质的量的关系为 ,两溶液中c (F-) c (CH3COO-)。
(4)25℃时,4.0×10-3mol・L-1HF溶液与4.0×10-4 mol・L-1 CaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生。
参考答案:(1)Cu(OH)2(2分), Cu2++2NH3・H2O=Cu(OH)2 ↓+2NH4+(2分)
(2)Ka=0.4×10-3或10-3.45。(3分)
HF电离平衡常数Ka= 【c(H+)c(F-)】/ c(HF),其中c(H+)、c(F-)、c(HF)都是电离达到平衡时的浓度,选择中间段图像求解。根据图像:PH=4时,c(H+)=10-4,c(F-)=1.6×10-3、c(HF)=4.0×10-4, Ka=0.4×10-3。(或根据a点数据c(H+)=10-3.45 、c(F-)=c(HF)得Ka= 10-3.45)(2分)
(3)>,= ,>(3分)
(4)PH=4.0,则c(H+)=10-4,此时:根据HF电离产生的c(F-)=1.6×10-3,而溶液中的c(Ca2+)=2.0×10-4。c 2(F-)×c(Ca2+)=5.12×10-10,5.12×10-10大于Ksp(CaF2)= ,此时有少量沉淀产生。(3分)
,此时有少量沉淀产生。(3分)
本题解析:略
本题难度:一般
3、填空题 I .用序号回答下列各题:
① 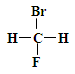 和
和 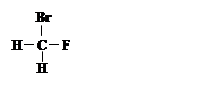
②1H―、2H、3H +、D2 ③淀粉和纤维素
④ 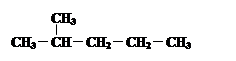 和
和
⑤16O2、18O3 ⑥235U、238U
其中互为同位素的是 。
互为同素异形体的是 。
互为同分异构体的是 。
是同一种化合物的是 。
II. 请选择合适的试剂检验某物质中是否含括号内物质:
序号
| 原物质(需检验物质)
| 试剂
|
①
| CO2(SO2)
|
|
②
| 乙醇(水)
|
|
③
| 直馏汽油( 裂化汽油)
|
|
Ⅲ.某元素R气态氢化物化学式为HnR。若最高价氧化物对应水化物分子中有b个氧原子,则其最高价氧化物对应水化物化学式通常表达为 。(含n和b)
参考答案:I、⑥⑤④①
II、①品红(或溴水或酸性高锰酸钾溶液)②CuSO4 ③溴水
III、H2b+n-8ROb
本题解析:I位素:质子数相同中子数不同的同一元素的原子互称同位素;
同素异形体:同种元素组成的不同单质;
同分异构体:分子式相同结构不同的化合物;
同一物质:组成和结构都相同的物质为同一物质,同一物质组成、结构、性质都相同,结构式的形状及物质的聚集状态可能不同.⑥235U、238U质子数相同中子数不同,互为同位素;
⑤16O2、18O3是氧元素的不同单质,互为同素异形体;
④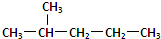 和
和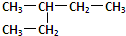 分子式相同结构不同,互为同分异构体;
分子式相同结构不同,互为同分异构体;
①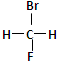 和
和 分子式相同,结构相同,是同一种化合物;
分子式相同,结构相同,是同一种化合物;
故答案为:⑥;⑤;④;①.
II. ①二氧化硫具有漂白性、还原性,二氧化碳不具有,则利用品红(或溴水或酸性高锰酸钾溶液)可检验,故答案为:品红(或溴水或酸性高锰酸钾溶液);
②无水硫酸铜遇水变蓝,则利用CuSO4可检验水的存在,故答案为:CuSO4;
③裂化汽油中含不饱和烃,而直馏汽油中含饱和烃,则利用溴水可检验裂化汽油,故答案为:溴水.
Ⅲ. 气态氢化物为HnR,说明其气态氢化物中化合价为-n,而在其最高价氧化物水化物中可知显8-n价,有气态氢化物说明显非金属性,且其最高价氧化物水化物分子中含b氧原子,其
化学式应符合HxROm,由化合物中化合价代数和为0,得x=0-【-2m+(8-a)】=2b+a-8,所以答案是H2b+n-8ROb
考点: 考查物质分类、物质检验的相关知识点以及考查学生根据化合价来书写化学式的知识
本题难度:一般
4、选择题 已知下列物质的名称分别是
名称
| 硫代硫酸钠
| 多硫化钙
| 过氧化钡
| 超氧化钾
|
化学式
| Na2S2O3
| CaSx
| BaO2
| KO2
|
根据上述命名规律回答:K2CS3应命名为
A.三硫代碳酸钾 B.多硫碳酸钾 C.过硫碳酸钾 D.超硫碳酸钾
参考答案:A
本题解析:K2CS3是碳酸钾K2CO3中的三个O原子被S原子代替得到的产物,应该名为三硫代碳酸钾,故选项是A。
考点:考查物质的命名的知识。
本题难度:一般
5、选择题 关于一些重要的化学概念有下列说法:①AgCl是一种难溶于水的电解质;②水玻璃是硅酸钠的俗名,也是电解质;③硝酸、纯碱、小苏打分别属于酸、碱、盐;④氧化还原反应都属于离子反应;⑤酸雨是指pH小于7.0的降水;?摩尔是国际科学界建议采用的七种基本物理量之一;⑦丁达尔效应可以区分溶液和胶体;⑧酸性氧化物:SiO2、NO2、SO3、NO;其中正确的是
A.①⑦
B.②⑦
C.③④
D.④⑤