1、选择题 下列各步制取物质,最终无法达到目的的有?
[? ]
A.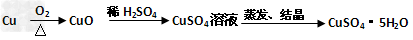
B.
C.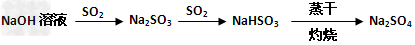
D.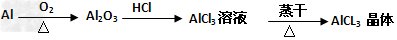
参考答案:D
本题解析:
本题难度:一般
2、实验题 CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。
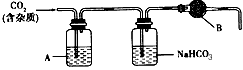
完成下列填空:
(1)用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol・L-1),应选用的仪器是____。
a.烧杯
b.玻璃棒
c.量筒
d.容量瓶
(2)上述装置中,A是____溶液,NaHCO3溶液可以吸收____。
(3)上述装置中,B物质是____ 。用这个实验得到的气体测定CO2的分子量,如果B物质失效,测定结果____(填“偏高”、“偏低”或“不受影响”)。
(4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:剪碎、称重 浸泡溶解
浸泡溶解 过滤
过滤 残渣烘干
残渣烘干 冷却、称重
冷却、称重 恒重
恒重
为了将石蜡和碳酸钙溶出,应选用的试剂是____。
a.氯化钠溶液
b.稀醋酸
c.稀硫酸
d.正己烷
(5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出_______ ,后溶出______。
(6)上述测定实验中,连续______________ ,说明样品已经恒重。
参考答案:(1)abc
(2)CuSO4溶液或酸性KMnO4溶液;HCl气体或酸性气体
(3)无水CaCl2 ;偏低
(4)bd
(5)石蜡;CaCO3
(6)两次称量的结果相差不超过(或小于)0.001 g
本题解析:
本题难度:一般
3、实验题 I 化学兴趣小组对用铜制取硫酸铜晶体的试验方案作研究。甲组同学将铜粉投入盛有稀硫酸的容器中,不发生反应。他们向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中放置些铂丝,反应速率明显加快。此时,其他组的同学提出方案如下:
乙组: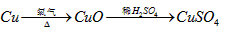
丙组: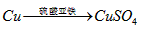
丁组: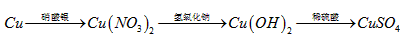
戊组: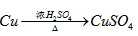
(1)甲组实验可用一个化学反应方程式表示为___________ ;使反应变快的可能原因是__________ ;从该反应器溶液(含有少量 以抑制水解)中取得产品的实验操作步骤应为_________ 、_______ 、__________ ,取得产品后的残留物质可循环使用。
以抑制水解)中取得产品的实验操作步骤应为_________ 、_______ 、__________ ,取得产品后的残留物质可循环使用。
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染。则在五组方案中,__________ 组方案最好。
II.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分解:
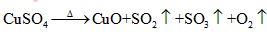 ,便决定设计实验测定反应生成的
,便决定设计实验测定反应生成的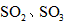 和O2的物质的量,并经计算确定该条件下
和O2的物质的量,并经计算确定该条件下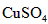 分解反应方程式中各物质的化学计量数。试验可能用到的仪器如下图所示:
分解反应方程式中各物质的化学计量数。试验可能用到的仪器如下图所示:
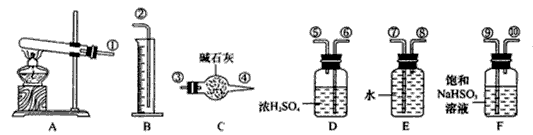
试验测得数据及有关结果如下;
① 准确称取6.0g无水;
②在试验结束时干燥管总质量增加2.4g;
③测得量筒中水的体积,得出气体在标准状况下的体积为280.mL;
试验结束时,装置F中的溶液只含NaHSO4和NaHSO3按装置从左到右的方向,各仪器接口连结顺序为: ①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(3)装置F的作用是__________。
(4)装置D的作用是__________。
(5)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温。 ②_____________ , ③________________ 。
(6)通过计算,推断出该条件下反应的化学方程式_______________________。
参考答案:I(1)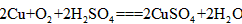 ;
;
形成了原电池;加热蒸发;冷却结晶;过滤并洗涤晶体。
(2)甲
Ⅱ(3)吸收放出等物质的量的
(4)干燥和
(5)②调节量筒使其液面与E装置中的液面持平;
③读量筒中液体体积时,视线与液体的凹液面相平。
(6)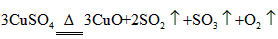
本题解析:
本题难度:一般
4、实验题 二氯化二硫(S2C12)在工业上用于橡胶的硫化。为了在实验室合成S2C12,某化学研究性学习小组查阅了有关资料,得到如下信息:
①在110℃ ~ 140℃时,将干燥的氯气与硫反应可得到S2C12的粗产品。
②有关物质的部分性质如下表:
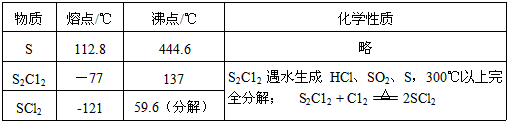
设计实验装置如下图:
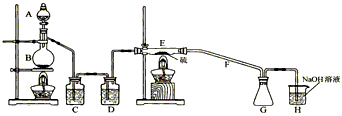
(1)①仪器A,B的名称分别为______________,______________。?
? ?②A中发生反应的离子方程式为____________________。
? ③C中的试剂名称是______________;仪器D的作用是_______________________。
(2)上图中装置不够完善,请你提出改进意见__________________________;
利用改进后的正确装置进行实验,请回答下列问题:
(3)E中反应的化学方程式为_____________________________________________。
(4)如果在加热E时温度过高,对实验结果的影响是_________________________,在F中可能出现的现象是_________________________________________。
(5)S2C12粗品中可能混有的杂质是____________、_____________、___________,为了提高S2C12的纯度,关键的操作是控制好温度和______________________。
参考答案:(1)①分液漏斗;蒸馏烧瓶
? ②MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
? ③饱和食盐水;除去氯气中少量的水蒸气
(2)在G和H之间增加干燥装置?
(3)2S+C12 S2C12
S2C12
(4)因副反应产率降低;有固体产生(答案合理即可)
(5)SCl2;C12;S;控制浓盐酸的滴速不要过快
本题解析:
本题难度:困难
5、简答题 如图所示,中学化学实验室采用该装置用于制备乙酸乙酯.
(1)写出制备乙酸乙酯的化学方程式______.
(2)浓硫酸在实验中的作用是______、______.
(3)加热一段时间后,在试管B饱和碳酸钠溶液的液面上方有一层油层,在油、水交界处观察到有气泡产生,气泡的主要成分是______.
(4)停止加热,取下试管B,嗅闻管内液体气味,闻到更多的是刺激性气味,这是因为物质的挥发等因素导致产品混有杂质,如______和______等,为进一步验证产物中某些杂质存在,在保持试管B相对稳定情况下,沿试管内壁滴入紫色石蕊试液,静置片刻会在试管内油层下方明显看到液体呈现三种颜色,由上而下分别为红色、紫色、蓝色,其原因可能是______,故产品需进行提纯.
(5)已知乙醇能和氯化钙结合.将所得产品依次用饱和碳酸钠溶液、饱和食盐水、饱和氯化钙溶液洗涤油层,分别分液.用饱和食盐水洗涤去除油层中可能含有的______杂质,减少乙酸乙酯的溶解,并防止对下面操作产生不利影响.
(6)在上述操作后,在所得油状液体中加入无水硫酸钠充分振荡,倾倒出油状液体,再进行______(填提纯的操作方法),收集74~78℃的馏分即可获得较纯净的乙酸乙酯.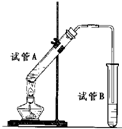
参考答案:(1)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,
故答案为:CH3COOH+CH3CH2OH

CH3COOCH2CH3+H2O
(2)乙酸与乙醇发生酯化反应,需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,浓硫酸的作用为催化剂,吸水剂,
故答案为:催化作用;吸水作用;
(3)水交界处观察到有气泡产生,气泡的主要成分是乙酸和碳酸氢钠反应生成的二氧化碳,故答案是:气体CO2;
(4)闻到的刺激性气味的物质是乙酸乙酯中混有的乙酸和乙醇;原因是:注入的石蕊试液快速降至油层下方,油层内含有的乙酸不断扩散溶解到下层的水溶液中,上层红色是因为乙酸浓度较高,中间紫色层是因为乙酸与碳酸钠反应接近中性,下层蓝色是因为碳酸钠溶液呈碱性;
故答案为:乙酸;乙醇;注入的石蕊试液快速降至油层下方,油层内含有的乙酸不断扩散溶解到下层的水溶液中,上层红色是因为乙酸浓度较高,中间紫色层是因为乙酸与碳酸钠反应接近中性,下层蓝色是因为碳酸钠溶液呈碱性;
(5)碳酸钠在饱和食盐水中易溶,乙酸乙酯溶解度减小,故选用饱和食盐水除去乙酸乙酯中的碳酸钠杂质,故答案为:碳酸钠;
(6)根据沸点不同,将混合液体分离的操作是蒸馏,通过蒸馏可以分离乙酸乙酯,故答案为:蒸馏.
本题解析:
本题难度:一般