1、填空题 以食盐为原料进行生产并综合利用的某些过程如下图所示。
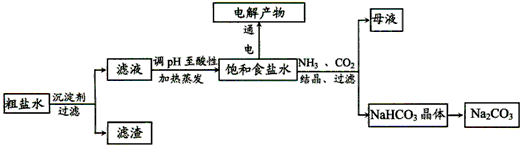
(1)除去粗盐中的Ca2+、Mg2+和SO42-离子,加入下列沉淀剂的顺序是(填序号)_________。
a.Na2CO3 b.NaOH c.BaCl2
(2)将滤液的pH调至酸性除去的离子是_________。
(3)电解饱和食盐水反应的离子方程式是_________。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是_________。
(5)纯碱在生产生活中有广泛的应用。
① 纯碱可用于除灶台油污。其原因是(结合离子方程式表述)__________________。
② 常温下,向某pH=11的Na2CO3溶液中加入过量石灰乳,过滤后所得溶液pH=13。则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是_________。
③ 工业上,可以用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是__________________。(已知碳酸的酸性强于次氯酸)。
参考答案:(1)cab或者cba或者bca
(2)CO32-和OH-
(3)2Cl- + 2H2O 2OH-+ H2↑ + Cl2↑
2OH-+ H2↑ + Cl2↑
(4)NH3
(5)①CO32-水解显碱性CO32-+ H2O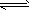 HCO3-+ OH-,油污在碱性条件下水解,达到去污目的;
HCO3-+ OH-,油污在碱性条件下水解,达到去污目的;
②1×1010;③2CO32-+ Cl2+H2O=Cl-+ClO-+2HCO3-
本题解析:
本题难度:一般
2、简答题 纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域.工业上以食盐、氨气(主要由合成氨厂提供)和二氧化碳为主要原料生产纯碱.其流程如下:根据以上信息回答下列问题.
(1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+、Mg2+等沉淀,可以向其中加入过量纯碱.此时将混合液中不溶物除去的方法是______;溶液中多余的纯碱可以加______试剂来除去.
(2)上述工艺流程中,加压条件下通入二氧化碳进行碳酸化时没有析出碳酸钠晶体,其原因是______.
(3)在氨碱工业的历史上,如何处理流程中剩余的滤液,出现了两种工艺:一是“索尔维法”,即在滤液中加入石灰水;二是我国化学家侯德榜发明的“联合制碱法”,即在滤液中加入适量氯化钠晶体.
①“索尔维法”中,滤液加石灰水前先要加热,原因是______.
②“联合制碱法”中,可以循环利用的物质是______?(用化学式表示).
(4)若采用上述流程生产106吨纯碱,则理论上通入的二氧化碳的体积(标准状况下)不得少于______L(不考虑二氧化碳的回收利用).

参考答案:(1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+、Mg2+等沉淀,可以向其中加入过量纯碱.此时将混合液中不溶物除去的方法是过滤,在滤液中加入盐酸到不再产生气体为止除去碳酸钠;
故答案为:过滤?盐酸;
(2)述工艺流程中,加压条件下通入二氧化碳进行碳酸化时没有析出碳酸钠晶体,是因为碳酸钠溶解度比碳酸氢钠大,所以不析出碳酸钠晶体;
故答案为:碳酸钠溶解度比碳酸氢钠大;
(3)①依据生产流程的过程分析,“索尔维法”中,滤液加石灰水前先要加热,由于滤液中还含有一定量的碳酸氢钠,加热时,碳酸氢根和铵根发生双水解反应,碳酸氢根转化为CO2而除去,防止加入石灰水时产生碳酸钙沉淀,故答案为:防止加入石灰水时产生碳酸钙沉淀;
②氯化钠溶液和氯化铵溶液中都含氯离子,氯化钠是制纯碱的原料,可以循环利用的 物质为氯化钠,故答案为:NaCl;
(4)若采用上述流程生产106吨纯碱,则理论上通入的二氧化碳的体积(标准状况下)不考虑二氧化碳的回收利用,可以根据化学方程式计算得到:
NH3+H2O+CO2+NaCl=NaHCO3↓+NH4Cl;2NaHCO3=Na2CO3+CO2↑+H2O;分析得到计算关系为:
2CO2~2NaHCO3~Na2CO3;
88? 106
88吨? 106吨
所以二氧化碳物质的量=88×106g44g/mol=2×106mol;
二氧化碳气体的体积=2×106mol×22.4L/mol=4,48×107L
4.48×107L;
故答案为:4.48×107
本题解析:
本题难度:一般
3、选择题 与氨碱法比较,下列关于联合制碱法优点的判断中不正确的是
[? ]
A.提高了原料的原子利用率
B.降低了生产成本
C.减少了环境污染
D.减轻了对设备的腐蚀
参考答案:D
本题解析:
本题难度:简单
4、填空题 【三选一化学与技术】
海水的综合利用,对于人类的生产生活有重要的意义。
(1)海水淡化沿海缺水地区获取淡水的方法之一,列举出海水淡化的两种方法_____________、________________。
(2)氯碱工业离子交换膜法生产中,透过离子交换膜的离子为_____________,氢氧化钠产生于____________(填‘“阳极”或“阴极”)。
(3)氯化钠为工业制纯碱的主要原料,制碱反应过程中法中析出NaHCO3的原因是______________;侯氏制碱法与索尔维制碱法相比除提高食盐利用率、无氯化钙生成的优势外还有______________?、_______________?从而综合利用原料、降低成本、减少环境污染。
参考答案:(1)蒸馏法 ;?电渗析法
(2)Na+;阴极
(3)氨化的饱和食盐水可大量的吸收CO2,从而产生大量的NaHCO3,而NaHCO3溶解度相对较小,从而饱和后析出;与合成氨联合生产;副产品氯化铵
本题解析:
本题难度:一般
5、填空题 [三选一选修2:化学与技术]
NaCl是价廉且应用广泛的化工业原料,例如,纯碱工业、氯碱工业、氯酸钾工业、肥皂工业等。 ?
(1)19世纪60年代氨碱法是纯碱工业广泛使用的方法,20世纪20年代以后被联合制碱法逐渐取代。?
①请写出以NaCl为原料利用氨碱法生产纯碱的化学方程式_______?; ?
②在联合制碱法中,纯碱工厂与__________工厂进行联合生产,以方便的获得原料____________?; ?
③在联合制碱法中循环使用,而在氨碱法中循环使用率不高的物质是____________。
(2)氯酸钾是重要的化工业产品,在火柴、炸药、雷管、焰火等制造中有重要应用,工业中首先通过电解热食盐水制得氯酸钠,再加入一定量的氯化钾即可得到氯酸钾沉淀。 ?
①在火柴、炸药、雷管、焰火的制造过程中大量使用氯酸钾,主要应用氯酸钾的_________性;
②请写出电解食盐水生产氯酸钠的化学方程式___________,该工艺过程中使用的装置与氯碱工业中使用的装置主要区别有______________(请答出两点); ?
(3)在肥皂的工业生成过程中,也要使用NaCl的目的是___________。
参考答案:(1)①?NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl? ,(或NH3+CO2+H2O=NH4HCO3?NH4HCO3+NaCl=NaHCO3↓+NH4Cl?)?2NaHCO3=?Na2CO3+CO2↑+H2O?
②?合成氨?;NH3、CO2?
③?CO2?,?NaCl?
(2)①?强氧化?(“氧化”也可)
?②?NaCl+3H2O NaClO3+3H2↑?; 需要加热恒温控制、没有离子交换膜?
NaClO3+3H2↑?; 需要加热恒温控制、没有离子交换膜?
(3)加入食盐使肥皂析出
本题解析:
本题难度:一般